
分析 (1)钠与水反应生成氢氧化钠和氢气2Na+2H2O═2NaOH+H2↑,该反应中钠失去电子0→+1,氢得到电子+1→0,转移2e-;
(2)Cu元素的化合价降低,C元素的化合价升高,转移的电子数为4e-.
解答 解:(1)钠与水反应生成氢氧化钠和氢气2Na+2H2O═2NaOH+H2↑,该反应中钠失去电子0→+1,氢得到电子+1→0,转移2e-,
则单线桥标出电子转移的方向和数目为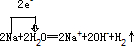 ,
,
故答案为: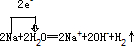 ;
;
(2)C+2CuO═2Cu+CO2↑中,氧化铜中Cu的化合价由+2价降到0价,一氧化碳中C的化合价由+2升高到+4价,一氧化碳是还原剂,氧化铜为氧化剂,双线桥法为: ,
,
故答案为:CuO;C; .
.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,注意电子转移的表示方法,侧重分析与应用能力的考查,题目难度不大.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源:2016-2017学年山西省高一上10月月考化学试卷(解析版) 题型:选择题
用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列图示对应的操作规范的是( )
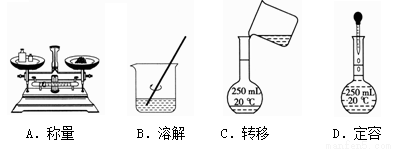
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
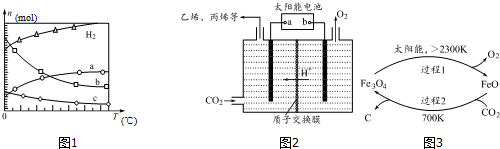
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 粒子 | I2 | Br2 | IO |
| 物质的量/mol | 0.5 | 1.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
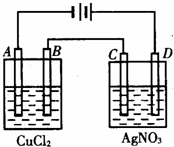 如图为以惰性电极进行电解:
如图为以惰性电极进行电解:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯碱溶液中逐滴加少量盐酸:CO32-+H+═HCO3- | |
| B. | 钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+ | |
| C. | 向FeBr2溶液中通入过量Cl2的离子方程式:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 过氧化氢能使酸性KMnO4溶液褪色:3H2O2+2MnO4-+6H+═2Mn2++4O2↑+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径A>B>C>D | B. | 原子序数D>C>B>A | ||
| C. | 离子半径C3->D->B+>A2+ | D. | 单质的还原性A>B>D>C |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
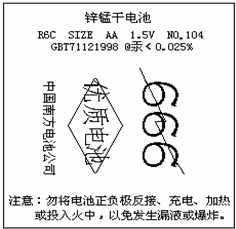 王亮在超市看到一种电池外壳的纸层包装印有如图的文字,请根据要求回答
王亮在超市看到一种电池外壳的纸层包装印有如图的文字,请根据要求回答查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com