
【题目】由硫酸的酸性强于碳酸可知:硫元素的非金属性强于碳元素,请再写出一事实也能说明硫元素的非金属性强于碳元素:__________。
科目:高中化学 来源: 题型:
【题目】通式为CnH2n-2的一种气态炔烃完全燃烧后,生成CO2和H2O的物质的量之比为4:3,则这种烃的链状同分异构体有( )
A.5种B.4种C.3种D.2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:

FeCl3溶液 /含有淀粉的碘水/NaOH溶液
A B C
(1)SO2气体还原Fe3+的氧化产物是____________(填离子符号),参加该反应的SO2和Fe3+的物质的量之比是____________。
(2)下列实验方案适用于在实验室制取所需SO2的是____________(填序号)。
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.铜与热浓H2SO4
(3)装置C的作用是_______________________________________。
(4)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、过滤、自然干燥,在这一系列操作中没有用到的仪器有____________(填序号)。
A.蒸发皿 B.石棉网 C.漏斗 D.烧杯 E.玻璃棒 F.坩埚
(5)在上述装置中通入SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第二份试液加入铁氰化钾溶液,产生蓝色沉淀。
方案②:往第一份试液中加入KMnO4溶液,紫红色褪去。
方案③:往第三份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是________,原因是__________________________________。
(6)能表明I-的还原性弱于SO2的化学方程式为__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在外加电场的作用下,氢氧化铁胶体粒子移向阴极的原因是
A. 铁离子带正电荷
B. 氢氧化铁带负电吸引阳离子
C. 氢氧化铁胶体粒子吸附阳离子而带正电荷
D. 氢氧化铁胶体吸附阴离子带负电荷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述中一定正确的是:
A. 30克SiO2中含有硅氧键个数为1NA
B. 常温常压下,1mol氦气含有原子数为NA
C. 1molO2与足量的金属钠完全反应得到电子数为2NA
D. 1mol甲基正离子(CH3+)所含电子数为9NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烯烃的甲酰化反应实例之一是CH3CH=CH2与CO、H2在催化剂作用下可合成正丁醛(CH3 CH2 CH2 CHO),有关反应如下:
①CH3CH=CH2(g)+CO (g)+H2(g)![]() CH3CH2CH2CHO(g) ΔH1
CH3CH2CH2CHO(g) ΔH1
副反应有:
②CH3CH=CH2(g)+ CO (g)+ H2(g)![]() (CH3)2CHCHO(g) ΔH2
(CH3)2CHCHO(g) ΔH2
③CH3CH=CH2(g)+ H2(g) → CH3 CH2 CH3(g) ΔH3
回答下列问题:
(1)不考虑副反应,则从绿色化学角度考虑,烯烃甲酰化反应的主要优点是_______________________________。
(2)已知下列键能数据:
化学键 | C-H | C-C | C=C | H-H |
键能/KJ·mol-1 | 413.3 | 347.7 | 615.0 | 436.0 |
则反应CH3CH=CH2(g)+ H2(g) → CH3 CH2 CH3(g)的ΔH3=_______________。
(3)在恒容密闭容器中充入1 mol丙烯,加入某种催化剂在加热条件下进行反应,测得温度与丙烯的总平衡转化率及两种异构体的物质的量之比的关系如下图所示:
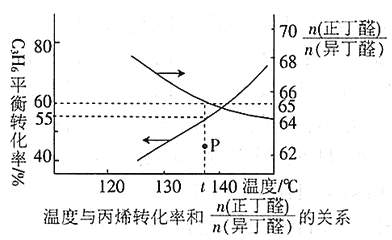
①丙烯合成正丁醛(CH3 CH2 CH2 CHO)及异丁醛((CH3)2CHCHO)的反应属于______________(填“吸热”或“放热”)反应。
②t℃时,反应(CH3)2CHCHO(g)![]() CH3 CH2 CH2 CHO(g)的平衡常数K =____________________,若发生上述反应①②,则反应达到平衡时,容器中正丁醛的物质的量为_______。
CH3 CH2 CH2 CHO(g)的平衡常数K =____________________,若发生上述反应①②,则反应达到平衡时,容器中正丁醛的物质的量为_______。
③t℃时,图中P点的反应速率v(正)_______v(逆)(填“<” “>”或“=”)。
④要提高正丁醛的产率除采用合适的温度外,还可_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com