
现有T、X、Y、Z短周期元素,其中T元素原子M层上有6个电子,X元素原子最外层电子数是次外层电子数的2倍,Y单质为双原子分子,其氢化物水溶液呈碱性,Z元素最高正价是+7价。
(1)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式 (用元素符号表示)
(2)元素Z与元素T相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 (填序号)。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(3)比较等浓度的Na2XO3溶液中c(XO32-)和NaHXO3溶液中c(HXO3-)大小,
c(XO32-) c(HXO3-)(填“>” “=”或“<”)
(4)A、J为常见的金属,G为T元素的最高价氧化物对应的水化物,B的溶液呈蓝色。
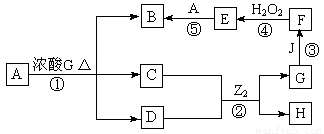
请回答下列问题:
①写出H的化学式____________________;
②写出反应①的化学方程式______________________________;
③写出酸性条件下反应④的离子方程式______________________________。
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | M层p电子数比s电子数多2个 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | M层上有2对成对电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下其单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z | 元素最高正化合价是+7 |
| H | + 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
现有T、X、Y、Z短周期元素,其中T元素原子M层上有6个电子,X元素原子最外层电子数是次外层电子数的2倍,Y单质为双原子分子,其氢化物水溶液呈碱性,Z元素最高正价是+7价。
(1)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式 (用元素符号表示)
(2)元素Z与元素T相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 (填序号)。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(3)比较等浓度的Na2XO3溶液中c(XO32-)和NaHXO3溶液中c(HXO3-)大小,
c(XO32-) c(HXO3-)(填“>” “=”或“<”)
(4)A、J为常见的金属,G为T元素的最高价氧化物对应的水化物,B的溶液呈蓝色。
请回答下列问题:
①写出H的化学式____________________;
②写出反应①的化学方程式______________________________;
③写出酸性条件下反应④的离子方程式______________________________。
查看答案和解析>>
科目:高中化学 来源:2012届天津市天津一中高三第二次月考化学试卷 题型:填空题
现有T、X、Y、Z短周期元素,其中T元素原子M层上有6个电子,X元素原子最外层电子数是次外层电子数的2倍,Y单质为双原子分子,其氢化物水溶液呈碱性,Z元素最高正价是+7价。
(1)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式 (用元素符号表 示)
示)
(2)元素Z与元素T相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 (填序号)。
(用元素符号表示),下列表述中能证明这一事实的是 (填序号)。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(3)比较等浓度的Na2XO3溶液中c(XO32-)和NaHXO3溶液中c(HXO3-) 大小,
大小,
c(XO32-) c(HXO3-)(填“>” “=”或“<”)
(4)A、J为常见的金属,G为T元素的最高价氧化物对应的水化物,B的溶液呈蓝色。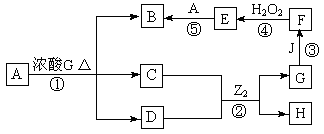
请回答下列问题:
①写出H的化学式____________________;
②写出反应①的化学方程式______________________________;
③写出酸性条件下反应④的离子方程式______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com