
【题目】烃类有机物在生活和生产中发挥着重要作用,研究它们意义重大。请回答下列问题:
(1)写出乙烷制氯乙烷的方程式______________________________,其反应类型为____________。
(2)写出以乙醇为原料经过两步反应制备乙烯的方程式,并指出第二步反应的反应类型。
第一步:__________________________________;
第二步:______________________,其反应类型为___________________。
(3)0.2mol某烃A在氧气中宋个燃烧后,生成CO2利H2O各1.2mol。若烃A不能使溴水褪色,但在一定条化下能与氯气发生取代反应,其一氯取代物有两种,则烃A的结构简式为___________________。
(4)在一定条件下,某些不饱和烃分子可以进行自身加成反应。例如:
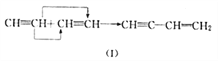
①参照(I)则有机物A![]() ,可由____________(填结构简式)相互加成制取。
,可由____________(填结构简式)相互加成制取。
②参照(I)当两分子丙烯发生自身加成时生成主链为4个碳原子的烃B,则B的结构简式为______,用系统命名法命名B_________________________。
【答案】 CH3CH3+Cl2![]() CH3CH2Cl+HCl 取代反应 CH2=CH2-OH
CH3CH2Cl+HCl 取代反应 CH2=CH2-OH![]() CH2=Cl2↑+H2O
CH2=Cl2↑+H2O ![]() 加聚反应
加聚反应 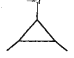 CH2=C(CH3)2 CH2=C(CH3)CH(CH3)2 2,3-二甲基-1-丁烯
CH2=C(CH3)2 CH2=C(CH3)CH(CH3)2 2,3-二甲基-1-丁烯
【解析】(1)乙烷在光照条件下与氯气反应生成氯乙烷,反应的化学方程式为:CH3CH3+Cl2![]() CH3CH2Cl+HCl;属于取代反应;(2)乙醇在浓硫酸催化下迅速加热至170°C生成乙烯和水,反应的方程式为:CH2=CH2-OH
CH3CH2Cl+HCl;属于取代反应;(2)乙醇在浓硫酸催化下迅速加热至170°C生成乙烯和水,反应的方程式为:CH2=CH2-OH![]() CH2=Cl2↑+H2O;乙烯在催化剂作用下发生加聚反应生成聚乙烯,反应的化学方程式为:
CH2=Cl2↑+H2O;乙烯在催化剂作用下发生加聚反应生成聚乙烯,反应的化学方程式为:![]() ; (3)0.2mol某烃A在氧气中宋个燃烧后,生成CO2利H2O各1.2mol,则烃的分子式为C6H12,烃A不能使溴水褪色,说明分子中没有碳碳双键。但在一定条件下能与氯气发生取代反应,其一氯取代物只有两种,这说明分子的氢原子只有两类,所以A是1,2,3-三甲基环丙烷,结构简式是
; (3)0.2mol某烃A在氧气中宋个燃烧后,生成CO2利H2O各1.2mol,则烃的分子式为C6H12,烃A不能使溴水褪色,说明分子中没有碳碳双键。但在一定条件下能与氯气发生取代反应,其一氯取代物只有两种,这说明分子的氢原子只有两类,所以A是1,2,3-三甲基环丙烷,结构简式是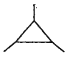 ;(4)①由信息可知,A中含1个碳碳双键,自身加成反应生成A,则为烯烃加成反应,碳链骨架不变,则A
;(4)①由信息可知,A中含1个碳碳双键,自身加成反应生成A,则为烯烃加成反应,碳链骨架不变,则A 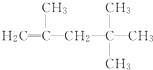 可由CH2=C(CH3)2相互加成制取;②当两分子丙烯发生自身加成时生成主链为4个碳原子的烃B,则双键C上的H发生加成反应,则B的结构简式为CH2=C(CH3)CH(CH3)2,用系统命名法命名为2,3-二甲基-1-丁烯。
可由CH2=C(CH3)2相互加成制取;②当两分子丙烯发生自身加成时生成主链为4个碳原子的烃B,则双键C上的H发生加成反应,则B的结构简式为CH2=C(CH3)CH(CH3)2,用系统命名法命名为2,3-二甲基-1-丁烯。


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
【题目】(1)根据元素周期律,碳的非金属性强于硅,请用一个化学反应方程式表示___________________。
(2)若FeSO4和O2的系数比为2∶1,试配平下列方程式:
![]() FeSO4+
FeSO4+![]() K2O2→
K2O2→![]() K2FeO4+
K2FeO4+![]() K2O+
K2O+![]() K2SO4+
K2SO4+![]() O2↑ __________________
O2↑ __________________
(3)各种氮氧化物(NO、NO2)是主要的大气污染物之一,治理氮氧化物(NOx)废气的方法之一是用NaOH溶液进行吸收,现有NO与NO2的混合气体,将其通入50 mL 2 mol/L的NaOH溶液中,恰好完全吸收,测得溶液中含有NO3- 0.02 mol。
①所得溶液中NaNO2的物质的量为________ mol;
②混合气体中V(NO)∶V(NO2)=________。
(4)As2O3俗称砒霜,As2O3是两性偏酸性氧化物,是亚砷酸(H3AsO3)的酸酐,易溶于碱生成亚砷酸盐,写出As2O3与足量氢氧化钠溶液反应的离子方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚氯乙烯(PVC)保鲜膜的安全问题引起广泛关注。PVC的安全隐患主要来自于塑料中残留的PVC单体以及不符合国家标准的增塑剂DEHA。工业上用乙烯和氯气为原料经下列各步合成PVC:
![]()
(1)乙是PVC的单体,其结构简式为_____________________;
(2)反应①的化学方程式为______________________________________________________;
(3)写出以下反应类型:反应②_________________;反应③_________________。
(4)邻苯二甲酸辛酯(DOP)是国家标准中允许使用的增塑剂之一,邻苯二甲酸( )是制造DOP的原料,它跟过量的甲醇反应能得到另一种增塑剂DMP(分子式为C10H10O4),DMP属于芳香酯,请写出DMP的结构简式为________________。
)是制造DOP的原料,它跟过量的甲醇反应能得到另一种增塑剂DMP(分子式为C10H10O4),DMP属于芳香酯,请写出DMP的结构简式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由一氧化碳、甲烷和乙烷组成的混合气体8.96L(标准状况),在足量氧气中充分燃烧后,生成气体先通过足量浓硫酸、再通过足量氢氧化钠溶液,测知氢氧化钠溶液增重26.4g,则原混合气体中乙烷的物质的量为
A. 0.1mol B. 0.2mol
C. 大于或等于0.2mo1,小于0.3mol D. 大于0.1mol,小于0.3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL的某稀H2SO4溶液中滴入0.1mol/L氨水,溶液中水电离出氢离子浓度随滴入氨水体积变化如图.下列分析正确的是
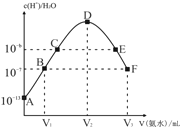
A. 稀硫酸的浓度为0.1mol/L
B. C点和E点溶液:pH=14-a
C. c(NH4+)/c(NH3·H2O);B点>F点
D. E溶液中存在c(NH4+)>c(SO42-)> c(OH-)> c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.皂化反应指的是油脂的酸性水解
B.葡萄糖和果糖互为同分异构体
C.部分蛋白质遇浓硝酸变黄色
D.驴皮熬制的阿胶中含有丰富的蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某离子反应涉及H2O、Cr2O72-、NO2-、H+、NO3-、Cr3+六种微粒,已知反应过程中NO3-浓度变化如图所示,且氧化剂和还原剂的物质的量之比为1∶3,下列判断错误的是( )
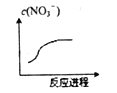
A. Cr2O72-中Cr化合价是+6 价 B. 反应的氧化产物是NO3-
C. 消耗1mol氧化剂,转移电子6mol D. 反应中Cr3+被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原电池的叙述中,正确的是( )
A.原电池的负极上发生还原反应
B.原电池工作时,电子总是由负极经导线流入正极
C.原电池中,正、负极的电极材料一定都是金属单质
D.酸碱中和反应也可以设计成原电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氧磷(POCl3)常用作半导体掺杂剂及光导纤维原料,实验室制备POCl3并测定产品含量的实验过程如下:
Ⅰ.制备POCl3。
采用氧气氧化液态PCl3法制取POCl3,实验装置(加热及夹持仪器略)如图所示:
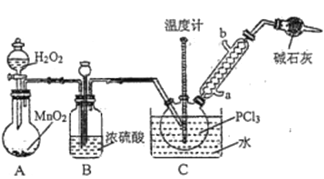
已知:①Ag++SCN-=AgSCN↓;Ksp(AgCl)>Ksp(AgSCN);磷酸银溶于硝酸。
②PCl3和POCl3的相关信息如下表:
物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
PCl3 | -112.0 | 76.0 | 137.5 | 两者互溶,均为无色液体,遇水均剧烈反应生成含氧酸和氯化氢 |
POCl3 | 2.0 | 106.0 | 153.5 |
(1)POCl3遇水反应的化学方程式为_________________________________________。
(2)装置B的作用除干燥O2外,还有_________________________________________。干燥管的作用是_______________。
(3)反应温度要控制在60~65℃,原因是_____________________________________________。
Ⅱ.测定POCl3产品的含量。
实验步骤:
①制备POCl3实验结束后,待三颈烧瓶中的液体冷却至室温,准确称取30.7gPOCl3产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100.00mL溶液。
②取10.00mL溶液于锥形瓶中,加入10.00mL3.2mol/LAgNO3标准溶液。
③加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖。
④以X为指示剂,用0.2mol/LKSCN溶液漓定过量的AgNO3溶液,达到滴定终点时共用去10.00mLKSCN溶液。
(4)步骤③中加入硝基苯的作用是___________________________________________。若无此操作,所测产品中氯元素的质量分数将会__________(填“偏大”、“偏小”或“不变”)。
(5)步骤④中X为__________,产品中POCl3的质量分数为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com