
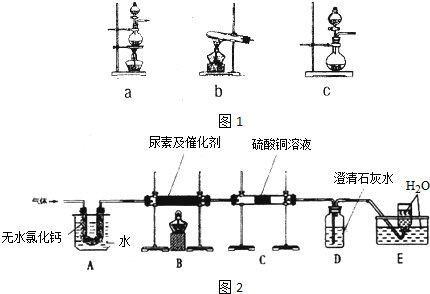
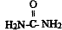 )做还原剂还原氮氧化合物是目前处理汽车尾气的一种方法,现设计实验模拟该过程并检验或收集其反应产物.
)做还原剂还原氮氧化合物是目前处理汽车尾气的一种方法,现设计实验模拟该过程并检验或收集其反应产物.| 3 |
| ||
| 3 |
| ||


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:
| A、反应后的溶液中不含Fe2+ |
| B、放出的NO气体的体积在标准状况为2.24L |
| C、稀硝酸的物质的量浓度为0.2mol?L-1 |
| D、所得溶液中Fe2+和Fe3+的物质的量之比为4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①④ | B、②③ | C、①③ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CH2CH=CH2+Br2→CH3- | |||
B、 +HNO3 +HNO3
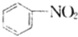 +H2O +H2O | |||
C、2CH3CH2OH+O2
| |||
D、CH3CH2OH+CH3COOH
|
查看答案和解析>>
科目:高中化学 来源: 题型:

| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 | |
| 第一次称量 | 第二次称量 | ||
| 11.710g | 22.700g | 18.621g | a |
查看答案和解析>>
科目:高中化学 来源: 题型:
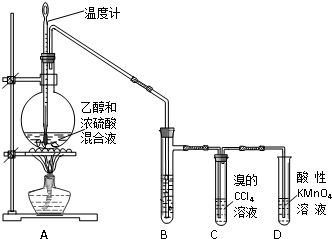
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com