
 某铵态氮肥由W、X、Y、Z 4种短周期元素组成,其中W的原子半径最小.
某铵态氮肥由W、X、Y、Z 4种短周期元素组成,其中W的原子半径最小. ;
; ;
;分析 某铵态氮肥由W、X、Y、Z等4种短周期元素组成,该铵盐中一定含有N、H元素,且W的原子半径最小,则W为H元素.
Ⅰ.若Y、Z同主族,ZY2是形成酸雨的主要物质之一,则ZY2为SO2,Y为O、Z为S元素,故X为N元素:
(1)X、Y、Z分别为N、O、S元素,分别处于第二周期ⅤA族、第二周期ⅥA族、第三周期ⅥA族;
(2)①N2H4分子中N原子之间形成1对共用电子对,N原子与H原子之间形成1对共用电子对;
②NH5为NH4H,由铵根离子与氢负离子构成;
③发生反应:4NH3+3O2═2N2+6H2O,计算4mol氨气反应放出的热量,注明物质聚集状态与反应热,书写热化学方程式;
Ⅱ.若Z是形成化合物种类最多的元素,则Z为C元素,
(4)该氮肥为碳酸铵或碳酸氢铵;
(5)a点时两种物质恰好完全反应,则c(HR)=$\frac{0.02L×0.25mol/L}{0.025L}$=0.2 mol/L,而HR溶液的pH=3,则HR为弱酸,NaR为强碱弱酸盐,溶液呈碱性,结合电荷守恒可知:c(R-)+c(OH-)-c(H+)=c(Na+);
②0.2 mol/L HR溶液中c(H+)=1.0×10-3mol/L,溶液中c(R-)≈c(H+),c(HR)≈0.2mol/L,代入电离常数Ka=$\frac{c({H}^{+})•c({R}^{-})}{c(HR)}$计算.
解答 解:某铵态氮肥由W、X、Y、Z等4种短周期元素组成,该铵盐中一定含有N、H元素,且W的原子半径最小,则W为H元素,
Ⅰ.若Y、Z同主族,ZY2是形成酸雨的主要物质之一,则ZY2为SO2,Y为O、Z为S元素,故X为N元素,
(1)X、Y、Z分别为N、O、S元素,分别处于第二周期ⅤA族、第二周期ⅥA族、第三周期ⅥA族,在周期表位置为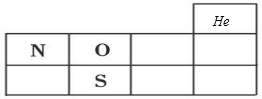 ,
,
故答案为: ;
;
(2)①N2H4分子中N原子之间形成1对共用电子对,N原子与H原子之间形成1对共用电子对,结构式为: ,
,
故答案为: ;
;
②NH5为NH4H,由铵根离子与氢负离子构成,电子式为 ,
,
故答案为: ;
;
③发生反应:4NH3+3O2═2N2+6H2O,4mol氨气反应放出的热量为382.8kJ×4=1531.2kJ,反应热化学方程式为:4NH3(g)+3O2(g)═2N2(g)+6H2O(l)△H=-1531.2 kJ•mol-1 ,
故答案为:4NH3(g)+3O2(g)═2N2(g)+6H2O(l)△H=-1531.2 kJ•mol-1 ;
Ⅱ.若Z是形成化合物种类最多的元素,则Z为C元素:
(4)该氮肥为碳酸铵或碳酸氢铵,
故答案为:碳酸铵或碳酸氢铵;
(5)a点时两种物质恰好完全反应,则c(HR)=$\frac{0.02L×0.25mol/L}{0.025L}$=0.2 mol/L,而HR溶液的pH=3,则HR为弱酸,NaR为强碱弱酸盐,R-离子水解,溶液呈碱性,则pH>7,则c(Na+)>c(R-),水解程度微溶,溶液中离子浓度为:c(Na+)>c(R-)>c(OH-)>c(H+),结合电荷守恒可知:c(R-)+c(OH-)-c(H+)=c(Na+)=$\frac{0.02L×0.25mol/L}{0.045L}$≈0.11mol•L-1,故ab错误、c正确,
故答案为:>;c;
②0.2 mol/L HR溶液中c(H+)=1.0×10-3mol/L,溶液中c(R-)≈c(H+)=1.0×10-3mol/L,c(HR)≈0.2mol/L,电离常数Ka=$\frac{c({H}^{+})•c({R}^{-})}{c(HR)}$=$\frac{1×1{0}^{-3}×1×1{0}^{-3}}{0.2}$=5.0×10-6,
故答案为:5.0×10-6.
点评 本题位置、结构与性质关系的综合应用,题目难度中等,涉及元素推断、电子式、结构式、热化学方程式、盐类水解、电离平衡常数等知识,试题知识点较多、综合性较强,侧重考查考生对基本概念和基本原理的理解和应用能力.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
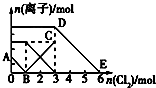 向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.有关说法不正确的是( )
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.有关说法不正确的是( )| A. | 线段BC代表Fe3+物质的量的变化情况 | |
| B. | 原混合溶液中n(FeBr2)=3mol | |
| C. | 当通入2molCl2时,溶液中已发生的离子反应为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- | |
| D. | 原溶液中n(Fe2+):n(I-):n(Br-)=2:1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当金属全部溶解时收集到NO气体的体积一定为2.24 L | |
| B. | 当生成的沉淀量达到最大时,消耗NaOH溶液的体积V≥100mL | |
| C. | 参加反应的金属的总质量3.6g<m<9.6 g | |
| D. | 当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 +3Fe+6HCl→
+3Fe+6HCl→ +3FeCl2+2H2O,产物苯胺还原性强,易被氧化,则由甲苯合成对氨基苯甲酸的步骤合理的是( )
+3FeCl2+2H2O,产物苯胺还原性强,易被氧化,则由甲苯合成对氨基苯甲酸的步骤合理的是( )| A. | 甲苯$\stackrel{硝化}{→}$X$\stackrel{氧化甲基}{→}$Y$\stackrel{还原硝基}{→}$对氨基苯甲酸 | |
| B. | 甲苯$\stackrel{氧化甲基}{→}$X$\stackrel{硝化}{→}$Y$\stackrel{还原硝基}{→}$对氨基苯甲酸 | |
| C. | 甲苯$\stackrel{还原}{→}$X$\stackrel{氧化甲基}{→}$Y$\stackrel{硝化}{→}$对氨基苯甲酸 | |
| D. | 甲苯$\stackrel{硝化}{→}$X$\stackrel{还原硝基}{→}$Y$\stackrel{氧化甲基}{→}$对氨基苯甲酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是通电后,将Co2+氧化成Co3+,然后以Co3+作氧化剂把水中的甲醇氧化成CO2而净化.实验室用如图装置模拟上述过程:
甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是通电后,将Co2+氧化成Co3+,然后以Co3+作氧化剂把水中的甲醇氧化成CO2而净化.实验室用如图装置模拟上述过程:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放.在一定温度下的2L固定容积的密闭容器中,通入2molCO2和3mol H2,发生的反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),△H=-a kJ•mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.
二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放.在一定温度下的2L固定容积的密闭容器中,通入2molCO2和3mol H2,发生的反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),△H=-a kJ•mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com