
【题目】某温度下,在容积为2 L的密闭容器中发生反应2X(g)+Y(g)![]() 2W(g) ΔH<0,当充入2 mol X和1 mol Y,经20 s达到平衡时生成了0.4 mol W。下列说法正确的是( )
2W(g) ΔH<0,当充入2 mol X和1 mol Y,经20 s达到平衡时生成了0.4 mol W。下列说法正确的是( )
①升高温度,W的体积分数减小,ΔH增大 ②以Y的浓度变化表示的反应速率为0.01 mol·L-1·s-1 ③在其他条件不变的情况下,增加1 mol X,则X和Y的转化率均提高 ④增大压强,正反应速率增大,逆反应速率减小,则平衡向正反应方向移动 ⑤再向容器中通入2 mol X和1 mol Y,达到平衡时,X、Y的转化率均增大
A. ⑤ B. ①⑤ C. ②③④ D. ④⑤
【答案】A
【解析】
①升高温度,W的体积分数减小,则平衡逆向移动,但ΔH不变,因为ΔH与方程式的写法有关,方程式确定, ΔH确定,错误;
②用W的浓度变化表示的反应速率v(W)=0.4/2×20=0.01 mol·L-1·s-1,根据速率之比和系数成正比,所以用Y表示的反应速率0.005 mol·L-1·s-1 错误;
③增加X的量,平衡正向移动,则X的转化率会减小,Y的转化率增大,错误;
④增大压强,正反应速率增大,逆反应速率也增大,但是正反应速率增加的程度大,则平衡向正反应方向移动,错误;
⑤再向容器中通入2molX和1molY,相当是对原平衡加压,平衡正向移动,达到平衡时,X、Y的转化率均增大,正确;
综上所述,本题选A。


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】乙烯产量是衡量一个国家石油化工水平的主耍标志。下图是由乙烯合成乙酸乙酯可能的合成路线:

请回答下列问题:
(1)反应④的化学方程式为_______________________________________________________。
(2)在实验室制备乙酸乙酯时,用到饱和的碳酸钠溶液,其作用是_____________________。
(3)乙醇的结构式为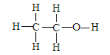 ,若实验证明乙醇分子有一个特殊氢原子的反应的化学方程式为_______________________________________。
,若实验证明乙醇分子有一个特殊氢原子的反应的化学方程式为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在H+、Mg2+、Fe2+、Fe3+、S2-、I-、S中,只有氧化性的是______________,只有还原性的是________________,既有氧化性又有还原性的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为元素周期表的一部分,根据元素a~j在周期表中的位置,按要求回答下列问题。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | a | |||||||
2 | b | c | d | e | ||||
3 | f | g | h | i | j | |||
(1)在a ~j中,化学性质最不活泼的元素是___________(填元素符号)。
(2)f、g、h的单质分别与水反应,最剧烈的是___________(填元素符号)。
(3)c、i的氢化物稳定性较强的是____________(填化学式)。
(4)c、f可形成既含离子键又含非极性键的化合物,该化合物的电子式为__________。
(5)d、f、g的离子半径最大的是_______________(填离子符号)。
(6)f的最高价氧化物的水化物与h的最高价氧化物的水化物反应的离子方程式为:___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关溶液的说法正确的是( )
A. pH相等的①NH4Cl、②NH4Al(SO4)2、③NH4HSO4溶液:浓度的大小顺序为①>②>③
B. HA的电离常数Ka =4.93×1010,则等浓度的NaA、HA混合溶液中:c(Na+) >c(HA) >c(A)
C. NaHCO3溶液加水稀释,c(Na+)与c(HCO3)的比值将减小
D. 已知在相同条件下酸性HF >CH3COOH,则物质的量浓度相等的NaF与CH3COOK溶液中:c(Na+) – c(F) >c(K+ ) c(CH3COO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像分别表示有关反应的反应过程与能量变化的关系。
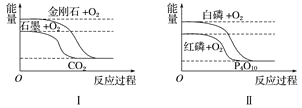
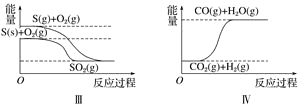
据此判断下列说法中正确的是( )
A. 石墨转变为金刚石是吸热反应 B. 白磷比红磷稳定
C. S(g)+O2(g)===SO2(g) ΔH1S(s)+O2(g)=SO2(g) ΔH2 则ΔH1>ΔH2 D. CO(g)+H2O(g)=CO2(g)+H2(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在固态金属氧化物电解池中,高温共电解H2O—CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示。下列说法不正确的是( )
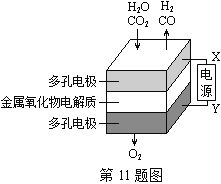
A. X是电源的负极
B. 阴极的反应式是:H2O+2eˉ=H2+O2ˉCO2+2eˉ=CO+O2ˉ
C. 总反应可表示为:H2O+CO2H2+CO+O2
D. 阴、阳两极生成的气体的物质的量之比是1︰1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com