
����Ŀ����֪��2-����-1��3-���������ٻ�ɫ���壬������ˮ����Һ�����ԣ��е�Ϊ88�棬����Ҫ��ҽҩ�м��塣ʵ���ҳ��Լ䱽����Ϊԭ�Ϸ����������ϳɣ�

����ʵ�鲽�����£�
�ٻǻ�����ȡ5.5g��ɷ�״�ļ䱽���ӷ����ձ��У���������Ũ���Ტ���Ͻ��裬�����¶�Ϊ60~65��Լ15min��
�����������ձ�������ˮ����ȴ�������ᣬ�����¶�(25��5) �����Ҽ�������15min��
��������Ӧ���������Բ����ƿB�У�С�ļ���������ˮϡ�ͣ��ټ���Լ0.1g���أ�Ȼ������ͼ��ʾװ�ý���ˮ�����������Һ��ȴ���ټ����Ҵ�-ˮ��ϼ��ؽᾧ��
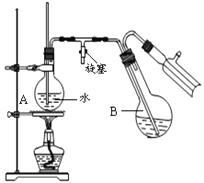
�ش��������⣺
��1��ʵ������Ƣ�������Ŀ����__________________________��
��2��������������ȡ�����ᡱ�ľ��������_________________________________________��
��3��д�������Ļ�ѧ����ʽ__________________________________________________.
��4����ƿA�в���������ѹ���ã����ܷ�ֹװ����ѹǿ���������¹ʣ�����_____________.
��5������ڵ��¶�Ӧ�ϸ���Ʋ�����30�棬ԭ����_________________________��
��6�����������2-����-1��3-���������Ժ��������ʣ����������Ҵ�-ˮ��ϼ�ϴ�ӡ�����Ƽ�ʵ��֤��2-����-1��3-�������Ѿ�ϴ�Ӹɾ���__________________________________________________��
��7����ʵ�����ջ��1.55g�ٻ�ɫ���壬��2-����-1��3-�����ӵIJ���ԼΪ___________��
���𰸡� ���⸱����IJ��� ����ƿ�м���������Ũ���ᣬ�����»�������һ������Ũ���ᣬ��ȴ 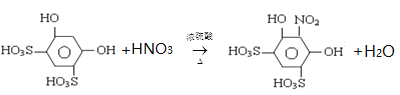 ��ֹѹǿ��С������ �¶Ƚϸ�ʱ�����ֽ�(��������)�����ʹ��� ȡ���һ��ϴ����Һ�������μ�BaCl2��Һ��������������֤���Ѿ�ϴ�Ӹɾ� 20%
��ֹѹǿ��С������ �¶Ƚϸ�ʱ�����ֽ�(��������)�����ʹ��� ȡ���һ��ϴ����Һ�������μ�BaCl2��Һ��������������֤���Ѿ�ϴ�Ӹɾ� 20%
�����������������(1). ʵ������Ƣ������ֱ�������������ȥ�����������2����ȡ�����ᡱ�ǰ�Ũ������Ũ����������Ũ����ϡ����ͬ����3���������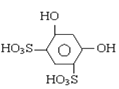 ��Ũ������Ũ����Ĵ������·���ȡ����Ӧ����
��Ũ������Ũ����Ĵ������·���ȡ����Ӧ����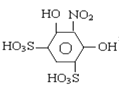 ����4��װ����ѹǿ����ʱ��������Һ��������װ����ѹǿ��Сʱ�����������ɲ����ܽ���װ������(5) �¶Ƚϸ�ʱ�����ֽ�����6��2-����-1��3-��������û��ϴ�Ӹɾ�����ϴ��Һ�к����������������7�����ݹ�ϵʽ
����4��װ����ѹǿ����ʱ��������Һ��������װ����ѹǿ��Сʱ�����������ɲ����ܽ���װ������(5) �¶Ƚϸ�ʱ�����ֽ�����6��2-����-1��3-��������û��ϴ�Ӹɾ�����ϴ��Һ�к����������������7�����ݹ�ϵʽ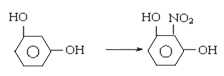 ����2-����-1��3-�����ӵIJ�����
����2-����-1��3-�����ӵIJ�����
������(1). ʵ������Ƣ������ֱ�������������ȥ�������������Ŀ���DZ������ɶ��������������������2����ȡ�����ᡱ�ǰ�Ũ������Ũ���������������������ƿ�м���������Ũ���ᣬ�����»�������һ������Ũ���ᣬ��ȴ����3��������� ��Ũ������Ũ����Ĵ������·���ȡ����Ӧ����
��Ũ������Ũ����Ĵ������·���ȡ����Ӧ����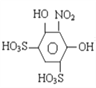 ������ʽ��
������ʽ�� ����4��װ����ѹǿ����ʱ��������Һ��������װ����ѹǿ��Сʱ�����������ɲ����ܽ���װ���У�������ƿA�в���������ѹ���ã����ܷ�ֹװ����ѹǿ���������¹ʣ����ܷ�ֹѹǿ��С��������(5). �¶Ƚϸ�ʱ�����ֽ�(��������)�����ʹ��������Բ���ڵ��¶�Ӧ�ϸ���Ʋ�����30������6��2-����-1��3-��������û��ϴ�Ӹɾ�����ϴ��Һ�к�����������ӣ�����ȡ���һ��ϴ����Һ�������μ�BaCl2��Һ��������������֤���Ѿ�ϴ�Ӹɾ�����7����2-����-1��3-�����ӵ����۲�����xg��
����4��װ����ѹǿ����ʱ��������Һ��������װ����ѹǿ��Сʱ�����������ɲ����ܽ���װ���У�������ƿA�в���������ѹ���ã����ܷ�ֹװ����ѹǿ���������¹ʣ����ܷ�ֹѹǿ��С��������(5). �¶Ƚϸ�ʱ�����ֽ�(��������)�����ʹ��������Բ���ڵ��¶�Ӧ�ϸ���Ʋ�����30������6��2-����-1��3-��������û��ϴ�Ӹɾ�����ϴ��Һ�к�����������ӣ�����ȡ���һ��ϴ����Һ�������μ�BaCl2��Һ��������������֤���Ѿ�ϴ�Ӹɾ�����7����2-����-1��3-�����ӵ����۲�����xg��

![]()
X=7.75g��2-����-1��3-�����ӵIJ���![]()


 �����Ļ�������ҵϵ�д�
�����Ļ�������ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������л��������ֽ���ǣ�������
A.NaHCO3B.Na2CO3C.H2SO4D.HC1O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���M�Ľṹ��ʽΪ�� �������й�������ȷ���� �� ��
�������й�������ȷ���� �� ��
A. �û��������NaHCO3��Һ��Ӧ�ų�CO2����
B. ����Ũ��ˮ��Ӧ��1 mol M�������4 mol Br2
C. ���Է����������ӳɡ�ȡ�����Ӿۡ����۷�Ӧ
D. ����NaOH��Һ��Ӧ��1 mol M�������3 mol NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯����[��FeCl3,Fe(OH)3,Na2FeO4��]��������������Ӧ�ù㷺��������ѧ֪ʶ���ش����⣺
��1�����ӹ�ҵ����30%��FeCl3��Һ��ʴ���ھ�Ե���ϵ�ͭ��������ӡˢ��·�壬����FeCl3��Һ��Fe3+���ڵij����Լ���_______��FeCl3��Һ��ʴ���ھ�Ե���ϵ�ͭ����Ӧ�����ӷ���ʽΪ________________�����Ӹ�ʴ��ķ�Һ�л���Cu�����»��FeCl3��Һ�����������Լ������������ۢ�Ũ�����������ռ�ް�ˮ����ѡ���Լ�______��д����Ӧ�����ӷ���ʽ����Һ�л���Cu_________����Һ���»��FeCl3��Һ_________��
��2����ˮ����μ���1mol/L FeCl3��Һ��������������Һ�����ĺ��ɫ���÷�Ӧ�Ļ�ѧ����ʽΪ____���÷�ɢϵ�з�ɢ�ʵ���ֱ��Ϊ____ nm��
��3����������Na2FeO4��һ�����;�ˮ��������ͨ�����·�Ӧ�Ƶ�2Fe(OH)3+3NaClO+4NaOH��2Na2FeO4+3X+5H2O��X�Ļ�ѧʽΪ____���ӻ��ϼ������Ƕȿ��ǣ����������ܹ�ɱ������Ϊ������____�ԡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڼ�����������������������γ��¡��ʻ�����ͬʱʧȥһ���Ӵ����÷�Ӧ�ƿ���ɭ(R��L��Claisen)�����Ϸ�Ӧ���䷴Ӧ�������£�2RCH2COOC2H5![]()
 +C2H5OH������Claisen��Ӧ�Ʊ�������H��һ�ֺϳ�·�����£�
+C2H5OH������Claisen��Ӧ�Ʊ�������H��һ�ֺϳ�·�����£�

�ش��������⣺
��1��A������Ϊ__________��C�Ľṹ��ʽΪ__________��
��2��F�к��������ŵ�������__________;��Ӧ���ķ�Ӧ������__________��
��3��E��F��Ӧ�Ļ�ѧ����ʽΪ_________________________________��
��4��B�ĺ��б�����ͬ���칹����_____________��(B��������)�����к˴Ź���������ʾ3���Ľṹ��ʽΪ__________��__________��
��5��������������( ![]() )��һ����Ҫ���л��ϳ�ԭ�ϣ�д�����Ҵ��Ʊ��������������ĺϳ�·��(���Լ���ѡ)��______________
)��һ����Ҫ���л��ϳ�ԭ�ϣ�д�����Ҵ��Ʊ��������������ĺϳ�·��(���Լ���ѡ)��______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������мȿ���Ũ�������ֿ��ù����������Ƹ������(����)
A.Cl2B.O2
C.SO2D.NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���ֽ����Ϊ̼�⻯���������̼�⻯����������ʵ�飺
����ȡһ������ȫȼ�գ�ʹȼ�պ������ͨ������ܣ����������0��72 g����ͨ��ʯ��ˮ��ʯ��ˮ����2��2 g��
�����ⶨ����̼�⻯����(����)���ܶ�����ͬ�����������ܶȵ�34����
����̼�⻯����0��1 mol�ܺ�32 g����ӳɷ�Ӧ��
�����������������������У���ԭ�ӷֲ��ڲ�ͬ��̼ԭ���ϣ������������һ��̼ԭ����֧���ϡ�
����˵����ȷ����
A. ��̼�⻯����Ϊ2-��-1��3-���ϩ
B. ��̼�⻯�������嵥��1:1�ӳ�ʱ��������3�ֲ�ͬ�IJ���
C. ��̼�⻯�������嵥��1:1�ӳ�ʱ��������2�ֲ�ͬ�IJ���
D. ��̼�⻯���������������ӳ�ʱ��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2016��7��22�վ�ɽй�飬�����л�̶��ദ���䱻��ˮ��û�����鷢���������з���վ������֯��ԮС�ӿ�չ�������߹����������������õ�ҩƷ������ǿ����ʵ���
A. Ư��B. ��ˮC. ˫��ˮD. ��ʯ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2017��3��21���ǵڶ�ʮ��조����ˮ�ա�������ˮ��Դ���������÷�ˮ��ʡˮ��Դ����ǿ��ˮ�Ļ��������ѱ�Խ��Խ���������ע����֪��ij��ɫ��ˮ�п��ܺ���H+��NH4+��Fe3+��Al3+��Mg2+��Na+��NO3����CO32����SO42���еļ��֣�Ϊ������ɷ֣��ֱ�ȡ��ˮ��Ʒ100 mL������������ʵ�飬��������й�ͼ��������ʾ��
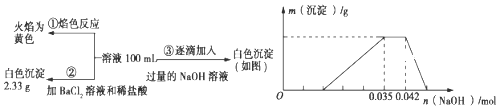
��ش��������⣺
��1����������3��ʵ����Է�����ˮ��һ�������ڵ���������_____��һ�����ڵ���������_____��
��2��д��ʵ���ͼ���г����ﵽ��������������ٷ����仯�η�����Ӧ�����ӷ�Ӧ����ʽ��_____��
��3������ͼ����ԭ��Һ��c��NH4+����c��Al3+���ı�ֵΪ_____�����ó��������������_____g��
��4����ͨ��ʵ��ȷ��ԭ��ˮ��c��Na+����0.14molL��1�����ж�ԭ��ˮ��NO3���Ƿ���ڣ�_____������ڡ��������ڡ���ȷ�������������ڣ�c��NO3������_____ molL��1�����������ڻ�ȷ����˿ղ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com