
����Ŀ��Burns��Dainton�о�����C12��CO�ϳ�COCl2�ķ�Ӧ�������£�
��C12��g��![]() 2C1��g����
2C1��g����
��CO��g��+C1��g��![]() COC1��g����
COC1��g����
��COC1��g��+C12��g��![]() COC12��g��+C1��g����
COC12��g��+C1��g����
���з�Ӧ�ڴ���v��=k��[CO][C1]��v��=k��[COC1]
����˵����ȷ���ǣ� ��
A.��Ӧ�ٵĻ�ܴ��ڷ�Ӧ�۵�
B.��Ӧ�ڵ�ƽ�ⳣ��K=![]()
C.Ҫ��ߺϳ�COCl2�����ʣ��ؼ�����߷�Ӧ�ڵ�����
D.ѡ����ʵĴ����ܼӿ�÷�Ӧ�����ʣ������COC12��ƽ�����
���𰸡�B
��������
������Ч��ײ���ۣ����ԽС����Ӧ����Խ�������ͷ�Ӧ�Ļ�ܣ���߷�Ӧ���ʣ������ı䷴Ӧ���յ�ƽ����ʡ�
A�����ԽС����Ӧ����Խ�죬��Ӧ�ٵĻ��С�ڷ�Ӧ�۵Ļ�ܣ���A����
B����Ӧ�ڴ���v��=k��[CO][C1]��v��=k��[COC1]��ƽ��ʱ���淴Ӧ������ȣ���![]() ����B��ȷ��
����B��ȷ��
C������Ӧ����������Ӧ���ʣ�Ҫ��ߺϳ�COCl2�����ʣ��ؼ�����߷�Ӧ�۵����ʣ���C����
D��������Ӱ��ƽ���ƶ�����ѡ����ʵĴ����ܼӿ�÷�Ӧ�����ʣ���COC12��ƽ����ʲ��䣬��D����
��ѡ��B��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������ҩ�� H��ͨ�����кϳ�·���Ʊ�
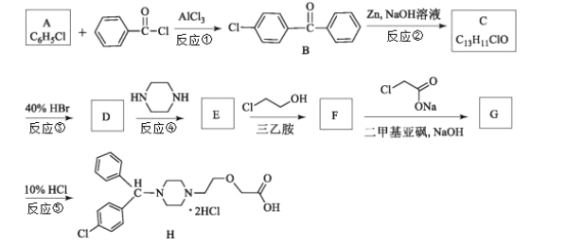
��֪: ![]() +NaH��
+NaH��![]() +HX��X Ϊ±��ԭ�ӣ�Nu-H Ϊ����ԭ�ӻ���ԭ�ӵĻ����
+HX��X Ϊ±��ԭ�ӣ�Nu-H Ϊ����ԭ�ӻ���ԭ�ӵĻ����
�ش��������⣺
(1)A��������_____����E��Ӧ������������_____��
(2)��Ӧ�ٺͷ�Ӧ�ڵķ�Ӧ���ͷֱ���_____�� _____��
(3)��Ӧ������ȡ����Ӧ��д��D�Ľṹ��ʽ ____��
(4)C�к��������ŵ�����Ϊ____��
(5)д����D����E�Ļ�ѧ��Ӧ����ʽ ____��
(6)д��������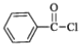 ��Ϊͬ���칹���ȩ�����Ľṹ��ʽ���˴Ź�������Ϊ����壬�������Ϊ1:1:1:1:1��_____��
��Ϊͬ���칹���ȩ�����Ľṹ��ʽ���˴Ź�������Ϊ����壬�������Ϊ1:1:1:1:1��_____��
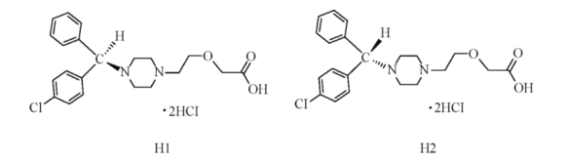
(7)����·�ߺϳɵ�H �����ֽṹH1��H2������H1�п��������ö�H2û�С�H1��H2����_____�칹�塣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������A�����ϣ��������к�C 72.0%��H 6.67%������Ϊ��������������֪A����Է�������Ϊ150���ִ����������л�������ķ��ӽṹ���������ַ�����
����һ���˴Ź����Dz��A�ĺ˴Ź���������5���壬�����֮��Ϊ1��2��2��2��3��
�����������ú�������ǿɳ�������л��������е�ijЩ���ţ��ֲ��A���ӵĺ��������ͼ��
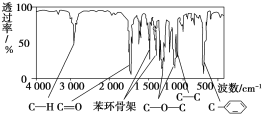
��֪��A������ֻ��һ���������ұ�����ֻ��һ��ȡ�������Իش��������⡣
(1)A�ķ���ʽΪ________��
(2)A�Ľṹ��ʽΪ_______________________________________________(дһ�ּ���)��
(3)A�ķ��㻯������ͬ���칹���ж��֣����з����в������ķ�����Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�У�����ȡ����Ӧ����
��CH3CH=CH2+Br2![]() CH3CHBrCH2Br
CH3CHBrCH2Br
��CH3CH2OH![]() CH2=CH2+H2O
CH2=CH2+H2O
��CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
��C6H6+HNO3![]() C6H5NO2+H2O
C6H5NO2+H2O
A. �٢�B. �ۢ�C. �٢�D. �ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��л���˵������ȷ����
A.CH3CH(OH)CH2COOHϵͳ������������3-�ǻ�����
B.��һ�������£�����Һ�塢Ũ���������屽���������ķ�Ӧ������ȡ����Ӧ
C.�ı�����ϩ��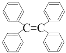 ��������̼ԭ��һ������ͬһƽ��
��������̼ԭ��һ������ͬһƽ��
D.1mol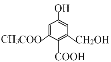 �ֱ���������Na��NaOH��Һ��NaHCO3��Һ��Ӧ���������������ʵ����ʵ����ֱ�Ϊ3mol��4mol��1mol
�ֱ���������Na��NaOH��Һ��NaHCO3��Һ��Ӧ���������������ʵ����ʵ����ֱ�Ϊ3mol��4mol��1mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʽ�Ȼ�ͭ[CuaClb(OH)c��xH2O]��һ��ɱ�����������ͨ�����²����Ʊ���
����1����ͭ�ۼ���ϡ�����У�������ͨ������Ӧ���� CuCl2����֪ Fe3+�Ը÷�Ӧ�д����ã����ԭ����ͼ��ʾ��
���� 2�����Ƶõ� CuCl2 ��Һ�У�����ʯ�����ַ�Ӧ���Ʊ���ʽ�Ȼ�ͭ��
�����й�˵����ȷ����
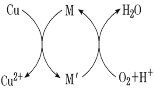
A.a��b��c֮��Ĺ�ϵʽΪ��a=b+c
B.ͼ�� M��M�@�ֱ�Ϊ Fe2+��Fe3+
C.���� 1 ��ַ�Ӧ�������� CuO ��Ϊ�˳�Fe3+
D.���Ʊ� 1 mol CuCl2������������ 11.2 L O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС�����ʵ�����ñ����ᣨ�е�249��������������е�82�����Ʊ���������������е�218������ʵ��װ����ͼ��
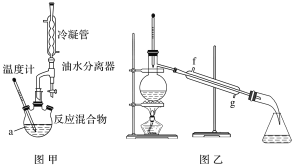
ʵ�鲽�裺����ͼ���������a�м��뷴Ӧ�ﱽ���ᡢ������ʹ���Ũ���ᣬ�ټ��뼸����ʯ���ڼ�����70 �����ң����ֺ��°�Сʱ���۽�����a�з�Ӧ���Һ����ͼ����ʾװ�ý��о��Ƶõ���Ʒ������˵������ȷ����
A.������a�м��������Լ����Ⱥ�˳���ǣ�Ũ���ᡢ�������������
B.����ı������������У���������DZ�����
C.ʵ�����ˮԡ���ȣ����¶ȹ���ʹ���ʼ�С
D.����۲���ʱӦ�ռ�218 ������֣�����¶ȼ�ˮ����ƫ�£����ռ��ľ��Ʋ�Ʒ�п��ܻ��е�����Ϊ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ɶ�����Ⱦ���γ�,���������PM2.5�����������NOx����CO��SO2�ȡ���ѧ�ڽ��������Ⱦ��������Ҫ�����á�
��1����֪:��![]() ��H1=-566.0 kJ��mol-1��
��H1=-566.0 kJ��mol-1��![]() ����H2=-116.5 kJ��mol-1��
����H2=-116.5 kJ��mol-1��![]() �� ��H3=+180.5 kJ��mol-1��������NO2 ��CO ת��������Ⱦ������Ȼ�ѧ����ʽΪ____��
�� ��H3=+180.5 kJ��mol-1��������NO2 ��CO ת��������Ⱦ������Ȼ�ѧ����ʽΪ____��
��2���о���������NH3�ɳ�ȥ���Ṥҵβ���е�NO��NH3��NO�����ʵ���֮�ȷֱ�Ϊ1��2��1��1.5��3��1ʱ,NO�ѳ������¶ȱ仯��������ͼ��ʾ��

������a��,NO����ʼŨ��Ϊ6��10-4mg��m-3,��X�㵽Y�㾭��10 s,���ʱ�����NO���ѳ�����Ϊ___________mg�� m-3��s-1��
������c��Ӧ��NH3��NO�����ʵ���֮����___,��������___��
��3��̿���������е���Ҫ������,�о����������Ի������,���ɻ��,������Կ�������SO2������̵������仯ģ���������ͼ��ʾ��
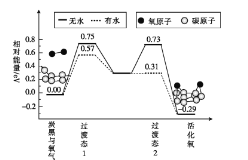
��ˮ�����,һ�������ӵĻ��Ϊ__��,��������ӵ�������___��������ˮ��������ˮ������
��4�����÷�Ӧ![]() ���ɵĵ�ؼ�����Ч��������������ŷ�,����������Ⱦ,���ܳ�����û�ѧ��,װ����ͼ��ʾ��
���ɵĵ�ؼ�����Ч��������������ŷ�,����������Ⱦ,���ܳ�����û�ѧ��,װ����ͼ��ʾ��
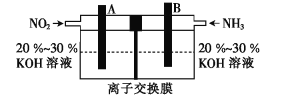
��B���ĵ缫��ӦʽΪ___��
������Ӧת��1.2 mol����,A������N2�����Ϊ___L����״������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڷ�ȼ�Ϻ��������У��ļ�����Ϊ���з���Ļ�ԭ�����㷺ʹ�á���UO2(NO3)-2HNO3-N2H4��HNO3��ϵ�²��õ�ⷨ�Ʊ��ļ��ˣ�����ܷ�ӦΪ2UO22++N2H5++3H+![]() 2U4++N2��+4H2O�����װ����ͼ��ʾ������˵����ȷ����
2U4++N2��+4H2O�����װ����ͼ��ʾ������˵����ȷ����

A.��ת��4mol e-������4mol H+�����ӽ���Ĥ
B.b���ĵ缫��ӦʽΪUO22+��2H2O��2e��=U4����4OH��
C.���Һ��NO3-���ƶ�����a�����ӽ���Ĥ��b
D.������11.2 mL N2ʱ��ͬʱ����U4+������Ϊ0.2389
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com