
【题目】强酸制弱酸非常重要的一种离子反应,已知:
Ka1 | Ka2 | |
H2SO3 |
|
|
H2CO3 |
|
|
下列离子反应不正确的有( )个
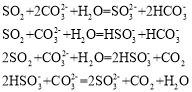
A.0个B.1个C.2个D.3个
【答案】B
【解析】
根据K大小得出酸强弱顺序为H2SO3 > H2CO3> HSO3- > HCO3-。由于H2SO3 >H2CO3> HSO3-,因此SO2 + CO32 + H2O = HSO3- + HCO3-,由于H2CO3 >HSO3- > HCO3-,因此HSO3- + CO32 = SO32 + HCO3-,两个方程式相加得到SO2 +2CO32 + H2O = SO32 + 2HCO3-,故第一个、第二个正确;由于H2CO3> HSO3-,因此SO2 + CO32 + H2O = HSO3- + HCO3-,由于H2SO3 > H2CO3,因此SO2 + HCO3- = HSO3- + CO2,两个方程式相加2SO2 + CO32 + H2O = 2HSO3- + CO2,故第三个正确;2HSO3- + CO32 = CO2+ H2O + 2SO32违背了H2CO3> HSO3-,故第四个错误,故B正确。
综上所述,答案为B。


科目:高中化学 来源: 题型:
【题目】常温下,向1L0.1 molL—l 一元酸HR溶液中逐渐通入氨气[已知常温下NH3 H2O电离平衡常数K = l .76x 10-5], 使溶液温度和体积保持不变, 混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是
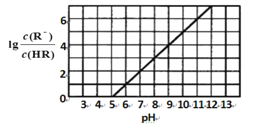
A.0. l molL—1HR 溶液的pH为5
B.HR为弱酸,常温时随着氨气的通入,c(R—)/[c(OH—).c(HR)] 逐渐增大
C.当通入0.1 mol NH3时,c(NH4+ > c(R—)
D.当c(R— )=c(HR)时 溶液必为中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子反应方程式正确的是( )
A.Fe(OH)3溶于稀 H2SO4 中:H++OH﹣→H2O
B.氨水滴入AlCl3溶液中:Al3++3OH﹣→Al(OH)3↓
C.FeO溶于稀HCl中:O2﹣+2H+→H2O
D.铝溶解在NaOH溶液中:2Al+2OH﹣+2H2O→2AlO2﹣+3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用反应TiO2(s)+CCl4(g) ![]() TiCl4(g)+CO2(g),在无水无氧条件下制取TiCl4,实验装置如图所示(CCl4、TiCl4的沸点分别为76 ℃、136 ℃,CCl4与TiCl4互溶)。下列说法正确的是
TiCl4(g)+CO2(g),在无水无氧条件下制取TiCl4,实验装置如图所示(CCl4、TiCl4的沸点分别为76 ℃、136 ℃,CCl4与TiCl4互溶)。下列说法正确的是
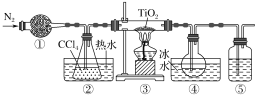
A.①、⑤分别盛装碱石灰、NaOH溶液
B.②中热水的作用是使CCl4汽化,④中冰水的作用是使TiCl4冷凝
C.③中反应结束后,先停止通N2,再停止加热
D.分离④中的液态混合物,采用的操作是分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向2.0L恒容密闭容器中充入1.0mol PCl5,反应PCl5(g)PCl3(g)+Cl2(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是( )
A.反应在50s时的速率v(PCl3)=0.0016molL﹣1s﹣1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11molL﹣1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,反应达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0molPCl3和2.0molCl2,达到平衡时,PCl3的转化率小于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成具有良好生物降解性的有机高分子材料是有机化学研究的重要课题之一。聚醋酸乙烯酯(PVAc)水解生成的聚乙烯醇(PVA),具有良好生物降解性,常用于生产安全玻璃夹层材料PVB。有关合成路线如图(部份反应条件和产物略去)。
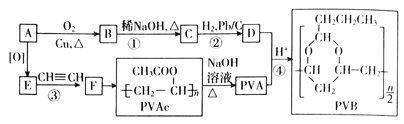
已知:I.A为饱和一元醇,其中氧的质量分数约为34.8%;
II.![]()
![]() ;
;
III.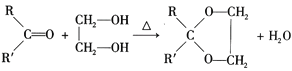 (R、R’可表示烃基或氢原子)
(R、R’可表示烃基或氢原子)
请回答:
(1)C中官能团的名称为_____________,写出C的反式异构体的结构简式:_______________,该分子中最多有______________个原子共面
(2)D与苯甲醛反应的化学方程式为_________________________________________________。
(3)③的反应类型是_________________________
(4)写出两种与F具有相同官能团的同分异构体的结构简式_____________________________。
(5)参照上述信息,设计合成路线,以溴乙烷为原料(其他无机试剂任选)合成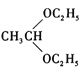 ,_____________
,_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂—空气电池充放电基本原理如图所示,电池装置中间用高分子隔膜隔开,下列说法不正确的是( )
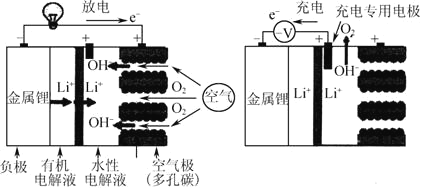
A.充电时,锂离子向阴极移动
B.充电时阴极电极反应式为Li++e- = Li
C.放电时正极电极反应式为O2+4e-+2H2O = 4OH-
D.电池装置中高分子隔膜允许水分子自由移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】传统的定量化学实验受到计量手段的制约而研究范围狭窄、精确度不高,DIS数字化信息系统(由传感器、数据采集器和计算机组成)因为可以准确测量溶液的pH等而在中和滴定的研究中应用越来越广泛深入。

(1)田老师利用DIS系统探究强碱和不同酸的中和反应,实验过程如下:
Ⅰ.分别配制0.1000mol/L的NaOH、HCl、CH3COOH溶液备用。
Ⅱ.用0.1000mol/L的NaOH溶液分别滴定10.00mL0.1000mol/L的HCl和CH3COOH溶液,连接数据采集器和pH传感器。
Ⅲ.由计算机绘制的滴定曲线如图一:
①A是_____;
②两曲线图中V1_____V2 (填“>”、“=”或“<”),A点和B点,水的电离程度相比_________(填“A大”、“B大”、“一样大”或“无法判断”)。
(2)程老师利用DIS系统测定某醋酸溶液的物质的量浓度,以测量溶液导电能力来判断滴定终点,实验步骤如下:用_____(填仪器名称)量取20.00mL醋酸溶液样品,倒入洁净干燥锥形瓶中,连接好DIS系统,如果锥形瓶中含有少量蒸馏水,是否会影响测量结果_____(填“是”、“否”或“不能确定”),向锥形瓶中滴加0.1000mol/L的NaOH溶液,计算机屏幕上显示出溶液导电能力与加入NaOH溶液体积关系的曲线图(见图二)。
①图中b点时,![]() _______mol/L
_______mol/L
②若图中某一点pH等于8,则c(Na+)﹣c(CH3COO﹣)的精确值为_____ mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水杨酸是合成阿斯匹林的重要原料。水杨酸的结构简式为![]()
请回答下列问题:
(1)请写出水杨酸中除苯环外具有的官能团的名称______________________;
(2)请写出与水杨酸互为同分异构体,既属于酚类又属于酯类化合物的结构简式:____________________________________________________;
(3)写出水杨酸与碳酸氢钠反应的化学方程式:______________________
(4)在一定条件下,水杨酸与乙酸酐可合成阿斯匹林,阿斯匹林如下图所示,1摩尔阿司匹林与氢氧化钠完全反应需要氢氧化钠_____摩尔。
![]()
(5)阿斯匹林药片需要保存在干燥处,受潮的药片易变质不宜服用;检验受潮药片是否变质的试剂是(只选一种试剂即可)_________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com