
【题目】碱式碳酸镁可用于牙膏、医药化妆品等工业,化学式为4MgCO3·Mg(OH)2·5H2O,某碱式碳酸镁中含有SiO2杂质,为测定其纯度。某兴趣小组设计了如下几个方案:
方案1
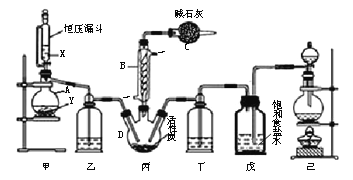
取一定质量的样品,与硫酸充分反应,通过测定CO2的质量计算纯度

(1)乙中发生反应的方程式为______________________________ 。
(2)仪器接口的连接顺序为(装置可以重复使用) a___________,丁的作用是__________________。
(3)关闭止水夹K,向样品中加入足量的稀硫酸,当样品充分反应完后,为了测定准确还应进行的操作是______________________________。
方案Ⅱ
①称取碱式碳酸镁样品mg;②将样品充分高温燃烧,冷却后称量;③重复操作②,测得剩余固体质量为m1g(用托盘天平称量)。
(4)下列仪器中,该方案不会用到的是____________。

(5)判断样品完全分解的方法是_________________________。
(6)有同学认为方案Ⅱ高温燃烧的过程中会发生![]()
会导致测定结果有误,你任为这位同学的观点正确吗?_________,(填“正确”或“错误”)
请说明自己的理由:______________________。
【答案】 4MgCO3·Mg(OH)2·5H2O+5H2SO4=5MgSO4+11H2O+4CO2↑ debcb 除去CO2中的水蒸气 打开止水夹K,缓慢通入空气 E 样品连续两次高温煅烧,冷却称量质量相差0.1g以内 错误 该反应的发生不影响生成CO2和水蒸气的量。
【解析】 (1)乙中4MgCO3·Mg(OH)2·5H2O与硫酸反应生成硫酸镁、二氧化碳和水,反应的化学方程式为4MgCO3·Mg(OH)2·5H2O+5H2SO4=5MgSO4+11H2O+4CO2↑,故答案为:4MgCO3·Mg(OH)2·5H2O+5H2SO4=5MgSO4+11H2O+4CO2↑;
(2) 根据实验目的,通过测定CO2的质量计算纯度,反应生成的二氧化碳中混有水蒸气,需要用浓硫酸的洗气瓶除去,然后用碱石灰吸收生成的二氧化碳,为了防止外界空气中的水蒸气和二氧化碳加入装置,需要在最后连接一个干燥装置,因此仪器接口的连接顺序为a debcb,其中丁的作用是除去CO2中的水蒸气,故答案为:debcb;除去CO2中的水蒸气;
(3)关闭止水夹K,向样品中加入足量的稀硫酸,当样品充分反应完后,为了测定准确,应该用不含有二氧化碳的空气将装置中的二氧化碳全部赶出,因此操作为打开止水夹K,缓慢通入空气,故答案为:打开止水夹K,缓慢通入空气;
(4)根据方案Ⅱ的步骤,将样品充分高温燃烧,用到酒精灯、三脚架、泥三角、坩埚,冷却后称量,用到干燥器,不会用到的仪器是蒸发皿,故选E;
(5) 样品连续两次高温煅烧,冷却称量质量相差0.1g以内,说明样品完全分解,故答案为:样品连续两次高温煅烧,冷却称量质量相差0.1g以内;
(6)根据反应![]() 可知,反应过程中的二氧化碳和水蒸气的量不变,对测定结果无影响,故答案为:错误;该反应的发生不影响生成CO2和水蒸气的量;
可知,反应过程中的二氧化碳和水蒸气的量不变,对测定结果无影响,故答案为:错误;该反应的发生不影响生成CO2和水蒸气的量;


科目:高中化学 来源: 题型:
【题目】生产、生活离不开化学.下列说法不正确的是( )
A.不需要通过化学反应就能从海水中获得食盐和淡水
B.油脂皂化生成的高级脂肪酸钠是肥皂的有效成分
C.聚乙烯塑料和聚氯乙烯塑料都是利用缩聚反应制得的
D.玻璃、陶瓷、水泥是重要的传统硅酸盐产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若两物质恰好完全反应,下列各项中反应前后保持不变的是( ) ①电子总数 ②原子总数 ③分子总数 ④物质的总能量 ⑤物质的总质量.
A.①③⑤
B.①②⑤
C.②③④
D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《神农本草经》说:“水银…镕化(加热)还复为丹.”《黄帝九鼎神丹经》中的“柔丹”“伏丹”都是在土釜中加热Hg制得的.这里的“丹”是指( )
A.氯化物
B.合金
C.硫化物
D.氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法中错误的是

A. 由红外光谱可知,该有机物中至少有三种不同的化学键
B. 由核磁共振氢谱可知,该有机分子中有三种不同化学环境的氢原子
C. 仅由A的核磁共振氢谱无法得知其分子中的氢原子总数
D. 若A的化学式为C2H6O,则其结构简式为CH3-O-CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 是合成高聚酚酯的原料,其合成路线(部分反应条件略去)如下图所示:
是合成高聚酚酯的原料,其合成路线(部分反应条件略去)如下图所示:

已知:

(1)A的结构简式为_____________,B的化学名称为_____________。
(2)由C生成D的反应类型为_____________。
(3)反应①的反应条件_____________。
(4)反应③的化学方程式为_____________。
(5)与D互为同分异构体且含有碳碳双键和-COO-的苯的二元取代物有_____种,其中核磁共振谱为5组峰,且峰面积比为2:1:2:2:1的结构简式为______________(任写一种)。
(6)写出以C2H5OH为原料合成乳酸( )的路线______________ (其他试剂任选,合成路线常用的表示方式为
)的路线______________ (其他试剂任选,合成路线常用的表示方式为![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关原电池的叙述正确的是( )
A. 原电池能将化学能转变为电能
B. 原电池的负极发生还原反应
C. 原电池在工作时,正极不断产生电子并经外电路流向负极
D. 原电池工作时,阳离子向负极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用现有三组溶液:①汽油和氯化钠溶液 ②汽油和柴油的混合物 ③从氯化钠和单质碘的水溶液中分离出碘,分离以上物质正确方法依次是( )
A.分液、蒸馏、萃取
B.萃取、蒸发、分液
C.分液、萃取、蒸馏
D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磺酰氯(SO2Cl2)是一种重要的有机合成试剂,实验室可利用SO2与Cl2在活性炭作用下反应制取少量的SO2Cl2,装置如下图所示(有些夹持装置省略)。已知SO2Cl2的熔点为-54.1 ℃,沸点为69.1 ℃,遇水能发生剧烈的水解反应,并产生白雾。
(1)单独检验己装置气密性的方法是:_______。
(2)由仪器B的使用可知SO2与Cl2反应的ΔH_______0(填“>”或“<”),仪器C的作用是_______。
(3)试剂X、Y的组合最好是________。
a.18.4 mol/L H2SO4+Cu b.4 mol/L HNO3+Na2SO3 c.60% H2SO4+K2SO3
(4)反应结束后,将丙中产物分离的实验操作是_______。
(5)分离产物后,向获得的SO2Cl2中加入足量NaOH溶液,振荡、静止得到无色溶液w。
①写出该反应的离子方程式:________;
②检验溶液w中存在Cl-的方法是________。
(6)SO2Cl2可以作为锂离子电池的正极活性材质,已知电池反应为:2Li+SO2Cl2=2LiCl +SO2↑。则电池工作时,正极的电极反应式为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com