
| A. | 把pH=2的甲酸溶液稀释100倍后pH=3.5 | |
| B. | 50mL l mol•L-1的甲酸溶液恰好与50mL l mol•L-1的NaOH溶液完全反应 | |
| C. | HCOONa溶液能使酚酞试液变红 | |
| D. | 0.1 mol•L-1的甲酸溶液的pH约为2 |
分析 强弱电解质的根本区别是电离程度,完全电离的电解质是强电解质,部分电离的电解质是弱电解质,只要能证明HCOOH部分电离就能证明HCOOH是弱电解质,据此分析解答.
解答 解:A.把pH=2的甲酸溶液稀释100倍后,如果甲酸是强酸,则稀释后溶液的pH=4,实际上稀释后溶液的pH=3.5,说明加水稀释促进甲酸电离,甲酸中存在电离平衡,为弱电解质,故A不选;
B.50mL l mol•L-1的甲酸溶液恰好与50mL l mol•L-1的NaOH溶液完全反应,说明甲酸是一元酸,但不能说明甲酸部分电离,所以不能说明甲酸为弱电解质,故B选;
C.HCOONa溶液能使酚酞试液变红,说明甲酸钠是强碱弱酸盐,则甲酸是弱酸,为弱电解质,故C不选;
D.0.1 mol•L-1的甲酸溶液的pH约为2,氢离子浓度小于酸浓度,说明甲酸存在电离平衡,为弱电解质,故D不选;
故选B.
点评 本题考查强弱电解质判断,为高频考点,明确强弱电解质根本区别是解本题关键,注意不能根据溶液导电性强弱、电解质溶解性强弱判断电解质强弱,为易错题,易错选项是B.


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 干燥的氯气能使湿润的有色布条褪色 | |
| B. | 影响气体体积大小的主要因素是微粒间的距离与微粒的大小 | |
| C. | 汤姆生发现原子中存在电子,并提出了“葡萄干面包式”原子结构模型 | |
| D. | 干冰升华的过程只需克服分子间作用力 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 装置①可用干石油的分馏 | |
| B. | 装置②可用于酒精提取溴水中的Br2 | |
| C. | 装置③可用于吸收HCl气体,并能防止倒吸 | |
| D. | 装置④验证乙烯的生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 235 g核素${\;}_{92}^{235}$U发生裂变反应:${\;}_{92}^{235}$U+${\;}_{0}^{1}$n$\stackrel{裂}{→}$${\;}_{38}^{90}$Sr+${\;}_{54}^{136}$U+10${\;}_{0}^{1}$n,净产生的中子( ${\;}_{0}^{1}$n)数为10NA | |
| B. | 60 g丙醇中存在的共价键总数为10 NA | |
| C. | 25 g质盆分数为68%的H202的水溶液中含氧原子数为NA | |
| D. | 2.0 g H218O与D2O的混合物中所含中子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项化合物 | A | B | C | D |
| Y | CuO | H2O | SiO2 | FeCl3 |
| W | H2O | Fe3O4 | CO | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2v(O2)=v(NO2) | |
| B. | 单位时间内生成n mol O2的同时生成2n molNO2 | |
| C. | 混合气体的颜色不再改变 | |
| D. | 混合气体的平均相对分子质量不再改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
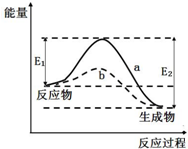
| A. | 该反应△H>0 | B. | a与b相比,a的反应速率更快 | ||
| C. | a与b相比,反应的平衡常数Ka=Kb | D. | 反应物总键能大于生成物总键能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验要求 | 所加试剂 | 主要操作 |
| 除去NaCl溶液中混有的I2 | 苯或四氯化碳 | 萃取、分液 |
| 除去NO气体中混有的NO2 | 水 | 洗气 |
| 除去SiO2固体中混有的Al2O3 | 盐酸 | 过滤 |
| 除去Fe2(SO4)3溶液混有的FeSO4溶液 | 过氧化氢 | ------ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com