
| A. | 浓硝酸保存在无色玻璃试剂瓶中 | |
| B. | 氢氧化钠溶液保存在带橡皮塞的玻璃试剂瓶中 | |
| C. | 少量的钠保存在煤油或石蜡油中 | |
| D. | 新制的氯水通常保存在棕色玻璃试剂瓶中 |
分析 A.依据浓硝酸见光分解的性质解答;
B.氢氧化钠能够与二氧化硅反应生成具有粘性的硅酸盐;
C.钠性质活泼易于空气中的水、氧气反应;
D.依据次氯酸见光分解的性质解答.
解答 解:A.浓硝酸见光分解,所以应保存在棕色瓶,故A错误;
B.氢氧化钠能够与二氧化硅反应生成具有粘性的硅酸盐,所以盛放氢氧化钠的试剂瓶不能用磨口玻璃塞,故B错误;
C.钠性质活泼易于空气中的水、氧气反应,钠密度大于煤油,可以用煤油或石蜡油中保存,隔绝空气,故C正确;
D.氯水中的次氯酸见光分解,所以氯水应保存在棕色玻璃试剂瓶中,故D正确;
故选:A.
点评 本题综合考查元素化合物知识,侧重于物质的保存的考查,为高频考点,注意物质的性质决定物质的保存方法,难度不大.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用清洁能源是防止酸雨发生的重要措施之一 | |
| B. | 推广“低碳经济”,减少温室气体的排放 | |
| C. | CO2、CH4、N2等均是造成温室效应的气体 | |
| D. | 利用晶体硅制作的太阳能电池可将太阳能直接转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
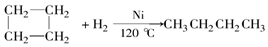
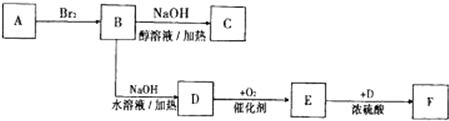
 ;C
;C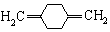 ;
;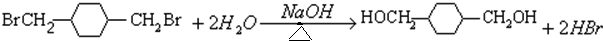 ;E→F:
;E→F: .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
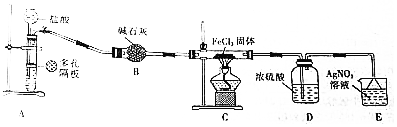
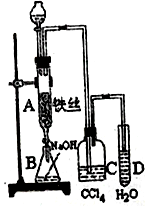 某学生在如图所示的装置中用苯和液溴制取溴苯,请根据下列实验步骤回答有关问题.
某学生在如图所示的装置中用苯和液溴制取溴苯,请根据下列实验步骤回答有关问题. ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 参加反应的Fe2+全部作还原剂 | |
| B. | 生成1.5molFe3O4时,反应转移电子 6mol电子 | |
| C. | 方程式中a=2 | |
| D. | 反应中被氧化的元素是Fe,被还原的元素是S和O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑤①③②④ | B. | ④②③①⑤ | C. | ①⑤③②④ | D. | ①⑤③④② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+、Fe3+、Cu2+ | B. | Fe2+、Cu2+、Fe3+ | C. | Cu2+、Fe2+、Fe3+ | D. | Fe3+、Cu2+、Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol/L的甲酸溶液中氢离子浓度约为10-2 mol/L | |
| B. | 甲酸能与水以任意比互溶 | |
| C. | 10 mol/L甲酸恰好与10 mol/LNaOH溶液完全反应 | |
| D. | 在一定温度下,甲酸的导电性比盐酸溶液弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com