
 如图所示的过程是目前直接利用太阳能的研究热点.人们把通过人工光化学手段合成燃料的过程叫做人工光合作用.
如图所示的过程是目前直接利用太阳能的研究热点.人们把通过人工光化学手段合成燃料的过程叫做人工光合作用.| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| n(CH3OH)/mol | 0.000 | 0.040 | 0.070 | 0.090 | 0.100 | 0.100 | 0.100 |
分析 (1)光合作用下生成燃料,燃料燃烧释放出能量;
(2)①根据v=$\frac{△c}{△t}$计算;
②达到平衡时正逆反应速率相等,各物质的浓度、含量不变;
(3)该原电池中,通入甲醇的电极是负极、通入氧气的电极是正极.
解答 解:(1)由据图可知,太阳能首先转化为化学能,其次化学能转化为热能,故答案为:热;
(2)①0~3min内甲醇的物质的量变化0.090mol,则v=$\frac{\frac{0.09mol}{2L}}{3min}$=0.015mol•L-1•min-1,
故答案为:0.015mol•L-1•min-1;
②a.v正(H2O)=2v逆(CO2),可说明正逆反应速率相等,达到平衡状态,故a正确;
b.无论是否达到平衡状态,生成物的物质的量之比都等于化学计量数之比,即n(CH3OH):n(O2)=2:3,故b错误;
c.因气体的体积以及质量不变,则容器内密度保持不变,不能用于判断是否达到平衡状态,故c错误;
d.反应前后气体的体积不等,容器内压强保持不变,可说明达到平衡状态,故d正确.
故答案为:ad;
(3)反应中甲醇被氧化,应为电池的负极,正极发生还原反应,氧气被还原生成水,电极方程式为O2+4H++4e-=2H2O,
故答案为:负;O2+4H++4e-=2H2O.
点评 本题考查化学反应与能量变化、化学平衡的相关计算以及原电池知识,为高频考点,侧重于学生的分析能力的考查,题目有利于培养学生良好的科学素养,提高学习的积极性,注意相关基础知识的积累.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 6和8 | B. | 20和17 | C. | 14和8 | D. | 6和16 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L0.1 mol•L-1盐酸和1L mol•L-1硫酸分别与1 L2 mol•L-1NaOH溶液反应速率相同 | |
| B. | 化学反应速率为0.8 mol•L-1•s-1,其含义是时间为1s时,某物质的浓度是0.8mol•L-1 | |
| C. | 0.1 mol•L-1硝酸与相同形状和大小的大理石反应的速率相同 | |
| D. | 对于任何化学反应来说,反应速率越大,反应现象就越明显 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.05 mol/(L•s) | B. | 0.10 mol/(L•s) | C. | 0.15 mol/(L•s) | D. | 2.0 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 |
| 完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 理论解释 | 结论 |
| A | H-N的键能大于H-P | 沸点:NH3>PH3 |
| B | 离子半径:Mg2+<Ba2+ | 热分解温度:碳酸镁髙于碳酸钡 |
| C | 离子半径:Na+<Cs+ | 配位数(C.N.):NaCl<CsCl |
| D | 晶格能:FeS2>ZnS | 岩浆中的硫化物矿物析出顺序ZnS先于FeS2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硫及其化合物对人类的生产和生活有着重要的作用.
硫及其化合物对人类的生产和生活有着重要的作用.| 实验 编号 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(SO2) | n(NO2) | n(NO) | ||
| 甲 | T1 | 0.80 | 0.20 | 0.18 |
| 乙 | T2 | 0.20 | 0.80 | 0.16 |
| 丙 | T2 | 0.20 | 0.30 | a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
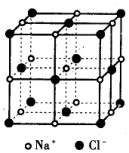 已知NaCl的摩尔质量为58.5g•mol-1,食盐晶体的密度为ρg•cm-3,若图中Na+与最邻近的Cl-的核间距离为a cm,那么阿伏加德罗常数的值可表示为( )
已知NaCl的摩尔质量为58.5g•mol-1,食盐晶体的密度为ρg•cm-3,若图中Na+与最邻近的Cl-的核间距离为a cm,那么阿伏加德罗常数的值可表示为( )| A. | 117α3ρ | B. | $\frac{M}{N{α}^{3}}$ | C. | $\frac{234}{{α}^{3}ρ}$ | D. | $\frac{58.5}{2{α}^{3}ρ}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 充电时,反应每生成1mol H+时电子转移的物质的量为1mol | |
| B. | 放电过程中,正极附近溶液的酸性减弱 | |
| C. | 放电时,正极反应为VO2++2H++e-═VO2++H2O | |
| D. | 充电时,阴极附近溶液由紫色逐渐变为绿色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com