
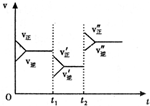
| A. | t1时若是降温使速率变化,则正确反应是放热反应 | |
| B. | t2时若是加压使速度变化,则A、B、C、D均为气体 | |
| C. | t2时改变的条件可能是加入催化剂 | |
| D. | t2时改变的条件可能是增大反应物的浓度 |
分析 A、t1时若是降温使速率变化,由图知正反应速率大于逆反应速率,平衡正向移动;
B、t2时若是加压使速度变化,由图知正反应速率大于逆反应速率,平衡正向移动,平衡正向移动;
C、t2时改变的条件可能是加入催化剂,则同等程度改变正逆反应速率,平衡不移动;
D、t2时改变的条件可能是增大反应物的浓度,逆反应速率在t2时刻不变.
解答 解:A、t1时若是降温使速率变化,由图知正反应速率大于逆反应速率,平衡正向移动,则正反应为放热反应,故A正确;
B、t2时若是加压使速度变化,由图知正反应速率大于逆反应速率,平衡正向移动,平衡正向移动,若A、B、C、D均为气体,加压应该逆向移动,故B错误;
C、t2时改变的条件可能是加入催化剂,则同等程度改变正逆反应速率,正逆反应速率相等,故C错误;
D、t2时改变的条件可能是增大反应物的浓度,逆反应速率在t2时刻不变,仍然等于t2时刻的速率,故D错误.
故选:A.
点评 本题考查化学反应速率与化学平衡的图象问题,根据温度、压强对反应速率的影响判断平衡移动的方向是解答该题的关键,注意压强对平衡移动的影响与化学计量数的关系,为易错点,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
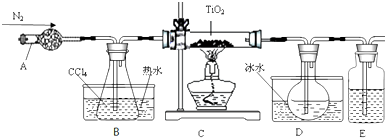
| 物质 | 熔点/℃ | 沸点/℃ | 其它 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳只存在金刚石和石墨两种同素异形体 | |
| B. | Mg、MgO中微粒的半径:r(O2-)>r(Mg2+)>r(Mg) | |
| C. | 在该反应条件下,Mg的还原性强于C的还原性 | |
| D. | 相同质量的镁在足量的CO2和O2中完全燃烧,固体质量增重相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
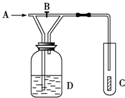 如图,从A处通入纯净的Cl2,打开B阀时,C处的红色布条上看不到明显现象;当关闭B阀后,C处红布逐渐褪色,则D瓶中装的是( )
如图,从A处通入纯净的Cl2,打开B阀时,C处的红色布条上看不到明显现象;当关闭B阀后,C处红布逐渐褪色,则D瓶中装的是( )| A. | 浓H2SO4 | B. | NaOH溶液 | C. | H2O | D. | 饱和NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该冶炼锌的反应属于置换反应 | |
| B. | 煤炭中起作用的主要成分是C | |
| C. | 冶炼Zn的反应方程式为:ZnCO3+2C$\frac{\underline{\;高温\;}}{\;}$Zn+3CO↑ | |
| D. | 倭铅是指金属锌和铅的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com