
进行污水处理分析时,常用双硫腙(H2Dz,二元弱酸)把金属离子络合成电中性的物质,再用CCl4萃取络合物,从而把金属离子从水溶液中完全分离出来。如用双硫腙(H2Dz)~CCl4分离污水中的Cu2+时,先发生络合反应:Cu2++2H2Dz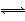 Cu(HDz)2+2H+,再加入CCl4,Cu(HDz)2就很容易被萃取到CCl4中。
Cu(HDz)2+2H+,再加入CCl4,Cu(HDz)2就很容易被萃取到CCl4中。
(1)写出双硫腙和Fe3+络合的离子方程式 ????????????????????????????????????????????????????? ,
萃取Fe3+的过程中要控制适宜的酸度,如果溶液的pH过大,其后果是 。
(2)如图是用双硫腙(H2Dz)~CCl4络合萃取某些金属离子的酸度曲线,它反映了萃取某些金属离子时适宜的pH范围。E%表示某种金属离子以络合物形式萃取分离的百分率。

某工业废水中含有Hg2+、Bi3+、Zn2+,用双硫腙(H2Dz)~CCl4络合萃取法处理废水。
①欲完全将废水中的Hg2+分离出来,须控制溶液的pH= 。
②当调节pH=2时,铋(Bi)的存在形式有 ,其物质的量之比为 。
③萃取到CCl4中的Zn(HDz)2分液后,加入足量NaOH溶液,充分振荡后,锌又转到水溶液中。写出反应的离子方程式: ?????????????????????????????????????????????????????
(3)污水中的亚汞离子(H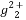 )必须转换成汞离子(Hg2+)才能用双硫腙络合。某工厂污水中含有较多的氯化亚汞(Hg2Cl2),加入二硫酸钾(K2S2O8)可氧化H
)必须转换成汞离子(Hg2+)才能用双硫腙络合。某工厂污水中含有较多的氯化亚汞(Hg2Cl2),加入二硫酸钾(K2S2O8)可氧化H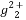 生成硫酸汞,写出该反应的化学方程式: 。
生成硫酸汞,写出该反应的化学方程式: 。
科目:高中化学 来源:山西省太原五中2011-2012学年高二上学期期末检测化学理科试题 题型:058
某铬盐厂生产过程中排出含Cr2O72-的工业酸性废水.为防止污染环境,现采用下列工艺流程进行处理后再排出.

在整个处理过程中,Cr2O72-被还原为Cr3+,溶液的pH值逐渐升高,最后滤出的沉淀有Cr(OH)3和Fe(OH)3,试分析这个污水处理过程,回答:
(1)电解时,铁电极上的电极反应式:
阳极:________,
阴极:________;
(2)用铁(而不用炭)作电极进行电解的原因:________;
(3)Cr2O72-在酸性环境中被还原剂还原,能除去Cr2O72-.减少溶液酸性是整个工艺流程中关键的一步,这个变化的离子方程式是________;
(4)电解过程中当H+浓度小到一定程度时,便会析出Cr(OH)3、Fe(OH)3沉淀,已知常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5 mol/L,溶液的pH应至少为________.
查看答案和解析>>
科目:高中化学 来源:学习周报 化学 人教课标高一版(必修1) 2009-2010学年 第12期 总第168期 人教课标版 题型:058
| |||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源:云南省同步题 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:
电浮选凝聚法是工业上采用的一种污水处理方法。
图1―6是电解污水实验装置示意图。接通直流电源后,与直流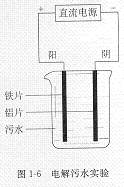 电源正极相连的阳极铁失去电子生成Fe2+,进一步被氧化,并生成Fe(OH)3沉淀,Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化的作用;与直流电源负极相连的阴极产生H2,气泡把污水中悬浮物带到水面形成浮渣层,积累到一定厚度时刮去(或撇掉)浮渣层,即起到了浮选净化的作用。
电源正极相连的阳极铁失去电子生成Fe2+,进一步被氧化,并生成Fe(OH)3沉淀,Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化的作用;与直流电源负极相连的阴极产生H2,气泡把污水中悬浮物带到水面形成浮渣层,积累到一定厚度时刮去(或撇掉)浮渣层,即起到了浮选净化的作用。
(1)根据该净化原理写出阳极区和阴极区上各自发生的电极反应式
阳极:
阴极:
(2)试分析不能参加反应的污染物是如何沉淀的:
(3)最后悬浮物为什么会形成浮渣:
(4)某同学甲模拟该原理进行污水处理实验,在电压符合要求情况下,发现产生气泡速率缓慢,无法使悬浮物形成浮渣。其原因是 。乙同学为甲同学提出一种切实可行的解决措施是向污水中加入适量的 溶液。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com