
| A. | 溶液密度ρ可表示为$\frac{cMr}{1000w}$ | |
| B. | 物质的量浓度c可表示为$\frac{ρV}{MrV+22.4m}$ | |
| C. | 溶液的质量分数w%可表示为$\frac{MrV}{22.4m}$ | |
| D. | 相对分子质量Mr可表示为$\frac{22.4m×w%}{(1-w%)V}$ |
分析 A、溶液的密度ρ=$\frac{溶液质量}{溶液体积}$,设溶液体积为VL,据此计算出溶液的密度;
B、.物质的量浓度c=$\frac{n}{V}$,先计算出溶液体积、溶质的物质的量,再计算出溶液的浓度;
C、根据溶质的质量分数=$\frac{溶质质量}{溶液质量}$×100%进行计算;
D、先计算出摩尔质量M=$\frac{m}{n}$,根据水的质量、溶质的质量分数计算出溶液的质量及溶质的质量,再计算出该化合物的相对分子量.
解答 解:A、设溶液的体积为VL,则溶液中溶质的质量为:m=cmol/L×VL×Mg/mol=cVM g,VL该溶液的质量为:$\frac{CVMr}{W%}g$,溶液的密度为:ρ=$\frac{\frac{CVMr}{W%}g}{1000VmL}$=$\frac{CM}{1000×W%}$g/mL,故A错误;
B、溶液体积为:V=$\frac{溶液质量}{溶液密度}$=$\frac{(\frac{MV}{22.4}+m)g}{ρg/mL}$=$\frac{MV+22.4m}{ρ}$mL,溶质的物质的量为:$\frac{VL}{22.4L/mol}$=$\frac{V}{22.4}$mol,该溶液的浓度为:c=$\frac{\frac{V}{22.4}mol}{\frac{MV+22.4m}{ρ×1{0}^{-3}L}}$=$\frac{1000ρV}{22.4(MV+22.4m)}$mol/L,故B错误;
C、溶液中溶质的质量为:m=nM=$\frac{VL}{22.4L/mol}Mg/mol$=$\frac{MV}{22.4}$g,溶液质量为:(m+$\frac{MV}{22.4}$g)g,则溶质的质量分数为:w%=$\frac{\frac{MV}{22.4}g}{\frac{MV}{22.4}g+mg}$=$\frac{MV}{22.4m+MV}$,故C错误;
D、质量分数为w%,则水的质量分数为:1-w%,水的质量为m,则溶液的质量为:$\frac{m}{1-W%}$g,溶质的质量为:$\frac{m}{1-W%}$g×w%,溶质的物质的量为:$\frac{VL}{22.4L/mol}$=$\frac{V}{22.4}$mol,则该化合物的摩尔质量为:$\frac{\frac{m}{1-W%}×W%g}{\frac{V}{22.4}mol}$=$\frac{22.4m×W%}{(1-W%)V}$g/mol,则该化合物的相对分子量为:M=$\frac{22.4m×W%}{(1-W%)V}$,故D正确;
故选D.
点评 本题考查了物质的量浓度、溶质质量分数、相对分子量、溶液密度的计算,题目难度中等,注意掌握物质的量浓度与溶质的质量分数的概念及计算方法,试题培养了学生灵活应用所学知识的能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 原子半径的大小顺序:r(W)>r(Z)>r(Y)>r(X) | |
| B. | Z2+可影响水的电离平衡 | |
| C. | Y的简单氢化物的热稳定性比W的弱 | |
| D. | Y分别与Z、W形成的化合物中化学键类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知A、B、C是中学化学的常见物质,它们在一定条件下有如图转化关系:
已知A、B、C是中学化学的常见物质,它们在一定条件下有如图转化关系:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
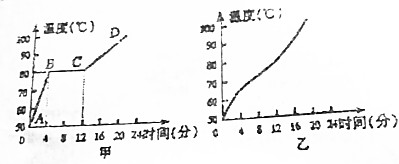
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | 只有① | C. | ②③ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com