


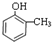
 ,则D为
,则D为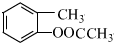 ,D用酸性高锰酸钾溶液氧化得到E.烃A与氯气在FeCl3催化剂条件下反应得到B,B发生水解反应、酸化得到C,则A为
,D用酸性高锰酸钾溶液氧化得到E.烃A与氯气在FeCl3催化剂条件下反应得到B,B发生水解反应、酸化得到C,则A为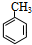 ,B为
,B为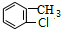 .E与氢氧化钠反应、酸化得到F为
.E与氢氧化钠反应、酸化得到F为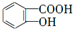 ,由信息(b)并结合抗结肠炎药物有效成分的结构可知,F在浓硫酸、浓硝酸加热条件下发生反应生成G为
,由信息(b)并结合抗结肠炎药物有效成分的结构可知,F在浓硫酸、浓硝酸加热条件下发生反应生成G为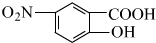 ,G发生还原反应得到抗结肠炎药物有效成分,据此解答.
,G发生还原反应得到抗结肠炎药物有效成分,据此解答. ,则D为
,则D为 ,D用酸性高锰酸钾溶液氧化得到E.烃A与氯气在FeCl3作催化剂条件下反应得到B,B发生水解反应、酸化得到C,则A为
,D用酸性高锰酸钾溶液氧化得到E.烃A与氯气在FeCl3作催化剂条件下反应得到B,B发生水解反应、酸化得到C,则A为 ,B为
,B为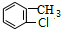 .E与氢氧化钠反应、酸化得到F为
.E与氢氧化钠反应、酸化得到F为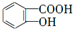 ,由信息(b)并结合抗结肠炎药物有效成分的结构可知,F在浓硫酸、浓硝酸加热条件下发生反应生成G为
,由信息(b)并结合抗结肠炎药物有效成分的结构可知,F在浓硫酸、浓硝酸加热条件下发生反应生成G为 ,G发生还原反应得到抗结肠炎药物有效成分,
,G发生还原反应得到抗结肠炎药物有效成分, ,故答案为:
,故答案为: ;
; ,
, .
.


科目:高中化学 来源: 题型:
| A、浊液的分散质可用过滤的方法从分散剂中分离开来 |
| B、任何物质在水中溶解时都有一定的溶解度 |
| C、淀粉溶液属于分散系中的溶液 |
| D、分散质粒子大小为几纳米到几十纳米的分散系是胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 常温下,用0.10mol?L-1 KOH溶液滴定10.00mL 0.10mol?L-1某二元弱酸H2R溶液所得滴定曲线如图(混合溶液总体积可看成混合前两种溶液体积之和).下列关系正确的是( )
常温下,用0.10mol?L-1 KOH溶液滴定10.00mL 0.10mol?L-1某二元弱酸H2R溶液所得滴定曲线如图(混合溶液总体积可看成混合前两种溶液体积之和).下列关系正确的是( )| A、点②所示溶液中:c(K+)+c(H+)=c(HR-)+c(R2-)+c(OH-) |
| B、点③所示溶液中:c(K+)>c(HR-)>c(H2R)>c(R2-) |
| C、点④所示溶液中:c(H2R)+c(HR-)+c(R2-)=0.04 mol/L |
| D、点⑤所示溶液中:c(H+)=c(HR-)+2c(H2R)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.25mol |
| B、0.2mol |
| C、0.15mol |
| D、0.1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| △ |


查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2H2(g)+O2(g)=2H2O (l)△H=-285.8 kJ?mol-1 |
| B、2H2(g)+O2(g)=2H2O (l)△H=+571.6 kJ?mol-1 |
| C、2H2(g)+O2(g)=2H2O (g)△H=-571.6 kJ?mol-1 |
| D、H2(g)+1/2O2(g)=H2O (l)△H=-285.8 kJ?mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com