
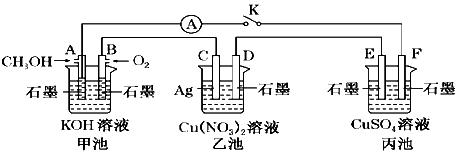
分析 甲池为燃料电池,A为负极,B为正极,则乙中C为阳极,D为阴极,阳极上Ag失电子生成银离子,阴极上铜离子得电子生成Cu,结合溶液中离子变化分析.
解答 解:(1)甲池为燃料电池,是原电池; A电极的电极是燃料发生氧化反应,反应式为CH3OH+8OH--6e-═CO32-+6H2O,故答案为:原电池;CH3OH+8OH--6e-═CO32-+6H2O;
(2)丙池中F与电源的负极相连是阴极,惰性电极电解硫酸铜生成铜和氧气,电极反应式为:2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2H2SO4+2Cu+O2↑,故答案为:阴极;2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2H2SO4+2Cu+O2↑;
(3)根据转移电子数目相等,4Ag~~O2,
4×108g 22400mL
4.32g V
所以$\frac{4×108g}{4.32g}=\frac{22400mL}{V}$,解之得:V=224mL,故答案为:224;
(4)甲池为燃料电池,A为负极,B为正极,则乙中C为阳极,D为阴极,阳极上Ag失电子生成银离子,阴极上铜离子得电子生成Cu,溶液中减少了Cu元素的质量,所以要让电解质复原,需要加入金属铜,故选:A.
点评 本题考查了原电池原理和电解池原理的应用,题目难度不大,侧重于考查学生的分析能力和对基础知识的应用能力,注意把握原电池和电解池中电极的判断以及电极上发生的反应.


科目:高中化学 来源: 题型:选择题
| A. | 5.8g由正丁烷与异丁烷组成的混合气体中含有的C-H键数目为NA | |
| B. | 将0.2mol NH3充入容器中加热分解,生成N2的分子数为0.1NA | |
| C. | 1L 0.1mol•L-1 NaHCO3溶液中HCO3-和CO32-数目之和为0.1NA | |
| D. | 当过量的铜与浓HNO3反应生成22.4L气体时,转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 50:3 | B. | 100:3 | C. | 50:6 | D. | 500:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Cl2发生氧化反应 | |
| B. | NH3是还原剂 | |
| C. | 每生成1 mol N2,转移3 mol电子 | |
| D. | 被氧化与未被氧化的NH3物质的量之比为1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 炼铁原料有铁矿石、焦炭、空气和石灰石 | |
| B. | FeCl3溶液能使KI淀粉溶液变蓝色 | |
| C. | 灼热的铁丝放入盛有干燥氯气的集气瓶中燃烧生成棕色的烟雾 | |
| D. | 利用Cu与FeCl3溶液的反应制作印刷电路板 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等温等压条件下,5 mol O2(g)和2 mol H2(g)的体积之比等于5:2 | |
| B. | 等温等压下,SO2气体与CO2气体的密度之比等于16:11 | |
| C. | 温度和容积相同的两气罐中分别盛有5 mol O2(g)和2 mol N2(g),压强之比等于5:2 | |
| D. | 温度相同、体积相同的O2(g)和N2(g)分子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 g H2和8 g O2 | |
| B. | 1 mol CO和22.4 L CO2 | |
| C. | 标准状况下,1.12 L N2和2.24 L He | |
| D. | 常温常压下,16 g O2和0.5 mol N2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com