
| A. | Li Na K | B. | Ba2+ Ca2+ Mg2+ | C. | Ca2+ K+ Cl- | D. | N O F |
分析 A.同主族自上而下原子半径增大;
B.离子电子层越多,离子半径越大;
C.离子电子层结构相同,核电荷数越大离子半径越大;
D.同周期自左而右原子半径减小.
解答 解:A.同主族自上而下原子半径增大,则原子半径大小为:Li<Na<K,故A正确;
B.离子电子层越多,离子半径越大,则离子半径大小为:Ba2+>Ca2+>Mg2+,故B错误;
C.离子电子层结构相同,核电荷数越大离子半径越小,则离子半径大小为:Ca2+<K+<Cl-,故C正确;
D.同周期自左而右原子半径减小,则原子半径大小顺序为:N>O>F,故D错误,
故选AC.
点评 本题考查了微粒半径大小比较,题目难度不大,明确粒子半径与电子层数、核电荷数的关系为解答关键,注意判断微粒半径时首先比较电子层数,电子层相同时再比较核电荷数.


科目:高中化学 来源: 题型:选择题
| A. | 酸性 HF>HCl>HBr>HI | B. | 热稳定性 HI>HBr>HCl>HF | ||
| C. | 单质活动性 F2>Cl2>Br2>I2 | D. | 离子还原性 F->Cl->Br->I- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
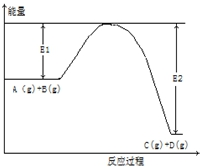 反应A(g)+B(g)?C(g)+2D(g)的能量变化如下图所示,回答下列问题.
反应A(g)+B(g)?C(g)+2D(g)的能量变化如下图所示,回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 互不相同 | B. | 在①和②中相同 | C. | 在②和③中相同 | D. | 在①②③中均相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
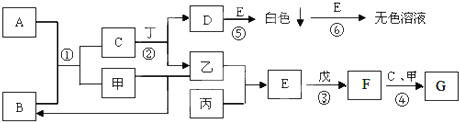
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V3>V1=V2 | B. | V3=V2>V1 | C. | V3>V2>V1 | D. | V1=V2>V3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水的颜色呈浅黄绿色,说明氯水中含有Cl2 | |
| B. | 向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- | |
| C. | 向氯水中加入NaHCO3粉末;有气泡产生,说明氯水中含有H+ | |
| D. | 氯水中加入氢氧化钠溶液,氯水的黄绿色消失,说明氯水中含有HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
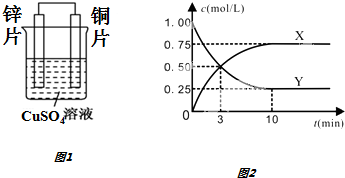
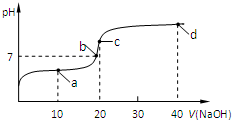
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com