
【题目】某兴趣小组用题图1装置(夹持装置略)收集某葡萄酒中SO2 , 并对含量进行测定. 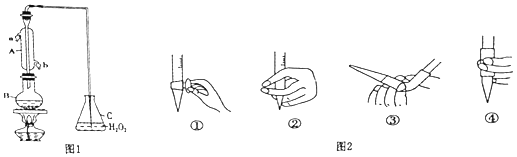
(1)仪器A的名称是 .
(2)B中加入300.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为 .
(3)除去C中过量的H2O2 , 然后用0.0900mol/LNaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的 .
(4)若滴定终点时溶液的pH=8.8,则选择的指示剂为 .
(5)该测定结果往往比实际值偏高,分析是由于采用试剂不当引起的,可能的原因为 .
【答案】
(1)冷凝管或冷凝器
(2)SO2+H2O2=H2SO4
(3)③
(4)酚酞
(5)盐酸易挥发
【解析】解:(1)根据仪器A的构造可知,仪器A为冷凝管,冷凝管中通水方向采用逆向通水法,冷凝效果最佳,所以应该进水口为b,
所以答案是:冷凝管或冷凝器;(2)双氧水具有氧化性,能够将二氧化硫氧化成硫酸,反应的化学方程式为:SO2+H2O2=H2SO4,
所以答案是:SO2+H2O2=H2SO4;(3)氢氧化钠溶液为碱性溶液,应该使用碱式滴定管,碱式滴定管中排气泡的方法:把滴定管的胶头部分稍微向上弯曲,再排气泡,所以排除碱式滴定管中的空气用③的方法,
所以答案是:③;(4)滴定终点时溶液的pH=8.8,应该选择酚酞做指示剂(酚酞的变色范围是8.2~10.0);
所以答案是:酚酞;(5)由于盐酸是挥发性酸,挥发的酸消耗氢氧化钠,使得消耗的氢氧化钠溶液体积增大,测定结果偏高;因此改进的措施为:用不挥发的强酸,如硫酸代替盐酸,或用蒸馏水代替葡萄酒进行对比实验,扣除盐酸挥发的影响,
所以答案是:盐酸易挥发.


科目:高中化学 来源: 题型:
【题目】铅蓄电池是典型的可充型电池,它的正负极是情性材料,放电时的电池总反应式为:Pb+PbO2+4H++2SO42-![]() 2PbSO4+2H2O。请回答下列问题,放电时正极的电极反应式是________________________;正极区pH值将____(填“变大”、“变小”或“不变”);电解液中H2SO4的浓度将_____(填“变大”、“变小”或“不变”);当外电路通过1mol电子时,理论上负极板的质量___(填“增加”或“减小”)________g。
2PbSO4+2H2O。请回答下列问题,放电时正极的电极反应式是________________________;正极区pH值将____(填“变大”、“变小”或“不变”);电解液中H2SO4的浓度将_____(填“变大”、“变小”或“不变”);当外电路通过1mol电子时,理论上负极板的质量___(填“增加”或“减小”)________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属铝在酸性或碱性溶液中均可与NO3-发生氧化还原反应,转化关系如下:
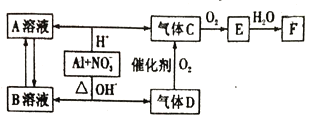
请回答下列问题:
(1) 气体D 与F 反应可生成盐,该盐的化学式为_________。
(2) C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C、E转化为无毒的气态单质,该单质的结构式是___________。
(3) 气体D转化为气体C 的化学方程式__________。
(4) Al 与NO3-在酸性条件下反应,Al与被还原的NO3-的物质的量之比是_____________。
(5) Al 与NO3-在碱性条件下反应的离子方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种以2 molL-1的Na2SO4溶液为电解质溶液的钠离子电池的总反应如下(P为+5价):NaTi2(PO4)3+Zn+Na2SO4![]() Na3Ti2(PO4)3+ZnSO4下列有关说法正确的是( )
Na3Ti2(PO4)3+ZnSO4下列有关说法正确的是( )
A. 放电时,NaTi2(PO4)3发生氧化反应
B. 放电时,Na+向锌棒一极移动
C. 充电时,阳极反应式为[Ti2(PO4)3]+-2e-=[Ti2(PO4)3]3+
D. 充电时,每转移0. 2 mol电子,阴极增重6.5 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示三个烧瓶中分别装人含酚酞的0.01mol/LCH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,向烧杯③中加入NH4NO3晶体,烧杯②中不加任何物质.则下列叙述正确的是( ) 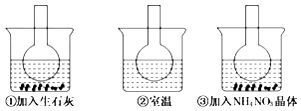
A.①说明水解反应为放热反应
B.③说明水解反应为吸热反应
C.①中溶液红色变浅
D.③中溶液红色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
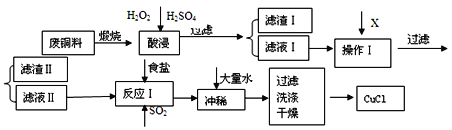
【题目】CuCl是有机合成的重要催化剂,并用于颜料、防腐等工业。工业上由废铜料(含Fe、Al及其化合物、SiO2杂质),生产CuCl的工艺流程如下:
物质 | 开始沉淀 | 沉淀完全 |
Fe(OH)3 | 2.7 | 3.7 |
Cu(OH)2 | 5.6 | 6.7 |
Al(OH)3 | 3.8 | 4.7 |
已知:CuCl溶于NaCl的浓溶液可生成CuCl2-,CuCl2-的溶液用水稀释后可生成CuCl沉淀。
(1)煅烧的主要目的是:______________________________________。
(2)操作Ⅰ为调节溶液的pH值,范围为___________,加入的物质X可以是_________________________ 。
A.CuO B.Cu(OH)2 C .NaOH 溶液 D.CaCO3
(3)滤渣I的主要成分是________,滤渣Ⅱ的主要成分是_________。
(4)往滤液Ⅱ中加入食盐并通入SO2可生成CuCl-,写出反应的离子方程式________________________________________________________________________________________ 。
(5)在反应Ⅰ中,加热并使用浓NaC1溶液,主要目的是_____________________________________________________________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用菱锰矿(MnCO3)[含FeCO3、SiO2、Cu2(OH)2CO3等杂质]为原料制取二氧化锰,其流程示意图如下:
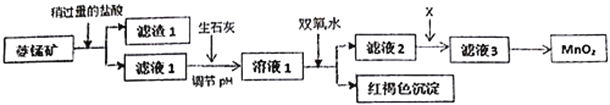
已知:生成氢氧化物沉淀的pH
Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
开始沉淀时 | 8.3 | 6.3 | 2.7 | 4.7 |
完全沉淀时 | 9.8 | 8.3 | 3.7 | 6.7 |
Ksp(CuS)=6.3×10-16 Ksp(MnS)= 3×10-14
注:金属离子的起始浓度为0.1 mol/L
回答下列问题:
(1)含杂质的菱锰矿使用前需将其粉碎,主要目的是_________________________。滤渣1的成分是_________,盐酸溶解MnCO3的离子方程式是_________________________________;
(2)用生石灰而不用NaOH调节pH的原因是_______________________________;
(3)滤液2中加入某种物质X可以除去Cu2+,最适合的是_______________;
A.MnO2 B.NaOH C.MnS
该反应的离子方程式是____________________________;
(4)将MnCl2转化为MnO2的一种方法是将酸化的NaClO3溶液氧化Mn2+,请补充并配平下列方程;____Mn2++_____ClO3-+______=____Cl2↑+____MnO2+_________;_________________
(5)将MnCl2转化为MnO2的另一种方法是电解法。(填“正极”或“负极”或“阴极”或“阳极”)
① MnO2在电解池的__________________(填“正极”或“负极”或“阴极”或“阳极”)生成;
② 若直接电解MnCl2溶液,生成MnO2的同时会产生少量Cl2。检验Cl2的操作是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知100℃时,水的离子积常数Kw=1×10-12,对于该温度下pH=l1的氨水,下列叙述正确的是
A. 向该溶液中加入同温同体积pH=1的盐酸,反应后溶液呈中性
B. 温度降低至25℃,该氨水溶液中H2O电离出的H+浓度小于10-11mol/L
C. 该氨水溶液中加入NH4Cl溶液,NH3·H2O的电离能力增强
D. 滴加等浓度等体积的硫酸,得到的溶液中存在电离平衡:NH4HSO4(aq)![]() NH4+(aq)+H+(aq)+SO42-(aq)
NH4+(aq)+H+(aq)+SO42-(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确且能达到相应实验目的的是
选项 | 实验目的 | 实验操作 |
A | 配制FeCl3溶液 | 将FeCl3固体溶解于适量蒸馏水 |
B | 称取2.0gNaOH 固体 | 先在托盘上各放一张滤纸,然后在右盘上添加2g 砝码,左盘上添加NaOH 固体 |
C | 检验溶液中是否含有NH4+ | 取少最试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 |
D | 验证铁的吸氧腐蚀 | 将铁钉放入试管中,用盐酸浸没 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com