
| A. | Na+的电子式: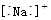 | B. | Na+的结构示意图: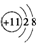 | ||
| C. | Na的电子排布式:1s22s22p63s1 | D. | Na的简化电子排布式:3s1 |
分析 A.钠离子为阳离子,其电子式中不需要标出最外层电子;
B.钠离子含有2个电子层,最外层含有8个电子;
C.钠原子含有11个电子,根据构造原理写出其电子排布式;
D.简化电子排布式只表示出最外层的电子排布式即可.
解答 解:A.Na+为简单阳离子,直接用离子符号表示其电子式,则钠离子的电子式为Na+,故A错误;
B.Na+的核电荷数为11,最外层满足8电子稳定结构,其离子结构示意图为: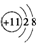 ,故B正确;
,故B正确;
C.Na的核外电子总数为11,其电子排布式为:1s22s22p63s1,故C正确;
D.Na的电子排布式为1s22s22p63s1,则其简化电子排布式:3s1,故D正确;
故选A.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及电子式、电子排布式、离子结构示意图等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.


科目:高中化学 来源: 题型:解答题
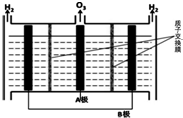
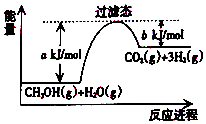 参考如图,按要求回答下列问题:
参考如图,按要求回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1 mol任何物质中都含有6.02×1023个分子 | |
| B. | 0.012 kg 12C中含有约6.02×1023 NA个碳原子 | |
| C. | 1 mol水中含有1 mol氢分子和1 mol氧原子 | |
| D. | 1 mol Ne中约含有6.02×1024个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 光照射甲烷和氯气的混合气体 | |
| B. | 乙烯通入溴水中 | |
| C. | 在镍作催化剂条件下,苯与氢气反应 | |
| D. | 苯与液溴混合后撒入铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | B. | Cu(OH)2+2HCl═CuCl2+2H2O | ||
| C. | 2Na+2H2O═2NaOH+H2↑ | D. | 2Na2O2+2CO2═2Na2CO3+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 NO能引起光化学烟雾,破坏臭氧层.处理NO有多种方法,根据题意回答下列问题:
NO能引起光化学烟雾,破坏臭氧层.处理NO有多种方法,根据题意回答下列问题:| 时间(s) | 0 | 1 | 2 | 3 | 4 | … |
| c(NO)/mol•L-1 | 1.00×10-3 | 4.00×10-4 | 1.70×10-4 | 1.00×10-4 | 1.00×10-4 | … |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com