
 ������Ԫ��X��Y��Z��������Ϊ1��7��12�γɵĻ����������������ӵ����ӷ�Ӧ����ʽ�ǣ�
������Ԫ��X��Y��Z��������Ϊ1��7��12�γɵĻ����������������ӵ����ӷ�Ӧ����ʽ�ǣ����� X��Y��ZΪ���ֶ�����Ԫ����ԭ��������������X��ԭ�Ӻ���ֻ��1�����ӣ���XΪHԪ�أ�Z��-2�����ӵĵ��Ӳ�ṹ���ʵ���ͬ����ZΪOԪ�أ�X��Yԭ�ӵ�����������֮�͵���Zԭ�ӵ���������������Y������������Ϊ5����YΪNԪ�أ��ݴ˽��
��� �⣺X��Y��ZΪ���ֶ�����Ԫ����ԭ��������������X��ԭ�Ӻ���ֻ��1�����ӣ���XΪHԪ�أ�Z��-2�����ӵĵ��Ӳ�ṹ���ʵ���ͬ����ZΪOԪ�أ�X��Yԭ�ӵ�����������֮�͵���Zԭ�ӵ���������������Y������������Ϊ5����YΪNԪ�أ�
��1������8�����ӡ�10�����ӵ�ԭ�ӵĻ�ѧ���ţ�188O���ʴ�Ϊ��188O��
��2������H��N��O����Ԫ����ɣ���Ũ��Һ��ʹ�������Ի�ɫ���ɴ˿�֪�Ļ�ѧʽΪHNO3���ʴ�Ϊ��HNO3��
��3����H��N��O����Ԫ���γɵĵ��ʻ����У������������Դ�ĵ����ǣ�H2��ͨ����������������N2������ʽΪ�� ��H��N��O��������Ϊ1��7��12�γɵĻ�������ԭ����Ŀ֮��Ϊ$\frac{1}{1}$��$\frac{7}{14}$��$\frac{12}{16}$=4��1��3���û�����ΪNH4NO3������NH4+�����ӵ����ӷ�Ӧ����ʽ�ǣ�NH4++OH-$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O��
��H��N��O��������Ϊ1��7��12�γɵĻ�������ԭ����Ŀ֮��Ϊ$\frac{1}{1}$��$\frac{7}{14}$��$\frac{12}{16}$=4��1��3���û�����ΪNH4NO3������NH4+�����ӵ����ӷ�Ӧ����ʽ�ǣ�NH4++OH-$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O��
�ʴ�Ϊ��H2��NH4++OH-$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��ƶ�Ԫ���ǽ���ؼ���ע��Ի���֪ʶ���������գ�


 һ��һ����ʱ���ϵ�д�
һ��һ����ʱ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �����ڷ���������c������ĸ�������뱽�Ĺ�ϵ��ͬϵ�д�������巢����Ӧ�Ļ�ѧ����ʽ
�����ڷ���������c������ĸ�������뱽�Ĺ�ϵ��ͬϵ�д�������巢����Ӧ�Ļ�ѧ����ʽ ��Ԥ��÷������ܣ���ܡ����ܡ����������෴Ӧ��
��Ԥ��÷������ܣ���ܡ����ܡ����������෴Ӧ��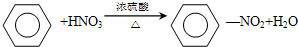 ������ȡ����Ӧ�����ɱ���ȡ�����飺
������ȡ����Ӧ�����ɱ���ȡ�����飺 �����ڼӳɷ�Ӧ��
�����ڼӳɷ�Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ͼ�У�PΪһ�����ɻ����Ļ������ر�K���ֱ�������A��B�и�����2molX��2molY����ʼʱ��VA=aL��VB=0.8aL����ͨ�ܵ�������Բ��ƣ�������ͬ�¶Ⱥ��д������ڵ������£��������и��Է���������Ӧ��
ͼ�У�PΪһ�����ɻ����Ļ������ر�K���ֱ�������A��B�и�����2molX��2molY����ʼʱ��VA=aL��VB=0.8aL����ͨ�ܵ�������Բ��ƣ�������ͬ�¶Ⱥ��д������ڵ������£��������и��Է���������Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ʱ�� ʵ����� | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 1 | 800�� | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800�� | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800�� | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | T | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѧ����һ�������� | |
| B�� | ��ѧ������ʹ���Ӽ����ϣ�Ҳ����ʹԭ�Ӽ����� | |
| C�� | ��ѧ��Ӧ�����з�Ӧ�ﻯѧ�����ѣ������ﻯѧ���γ� | |
| D�� | �Ȼ��ƹ�������ˮû����������������û���ƻ���ѧ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������������ͨ�����������Һ�У�SO2+H2O+3ClO-�TSO42-+Cl-+2HClO | |
| B�� | �ð�ˮ�ܽ��Ȼ���������Ag++2 NH3•H2O�T[Ag��NH3��2]++2H2O | |
| C�� | �ö��Ե缫���MgCl2��Һ��2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$Cl2��+H2��+2OH- | |
| D�� | �����ʵ�����Ba��OH��2�루NH4��2Fe��SO4��2����Һ�з�Ӧ��Ba2++2OH-+2NH4++SO42-�TBaSO4��+2NH3•H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ⱥ��ʳ��ˮʱ��������������Cl-����������Ӧ | |
| B�� | Ǧ���طŵ�ʱ�������������ᣬ������������ | |
| C�� | �����������������Ʋ������ʧȥ�������� | |
| D�� | ���������绯ѧ��ʴ�ĸ�����Ӧʽ��Fe-3e-�TFe3+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com