

 ;该反应的类型为取代.
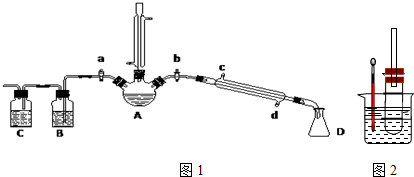
;该反应的类型为取代.分析 本题是对苯和液溴反应原理的探究,对课本实验进行了改进,涉及反应后的混合液的分离提纯和对实验过程中溴化氢的检验,反应混合物静置后分层可分液分离,得到的粗溴苯中仍混有的苯因混溶可通过蒸馏进一步分离,因溴的挥发,检验溴化氢时要先排除溴的干扰,并借助硝酸银溶液里有浅黄色沉淀来证明溴化氢的存在,同时还要注意尾气处理,
(1)苯与液溴在催化剂条件下发生取代反应生成溴苯;
(2)该反应中有溴化氢生成,溴化氢溶于水得到氢溴酸,氢溴酸能使石蕊试液变红色;氢溴酸能和硝酸银反应生成淡黄色沉淀溴化银;
(3)溴苯中的溴易挥发,非极性分子的溶质易溶于非极性分子的溶剂,有机物易溶于有机物,据此分析苯的作用;
(4)倒置漏斗或球形干燥管能防止溶液倒吸;
(5)溴化铁与氢氧化钠反应生成氢氧化铁沉淀,溴苯密度大于水,是无水油状液体,溴化氢易挥发;
(6)溴化氢能污染空气,不能直接排放到空气中
解答 解:(1)苯与液溴在催化剂条件下发生取代反应,方程式为: ,
,
故答案为: ;取代;
;取代;
(2)该反应中有溴化氢生成,溴化氢溶于水得到氢溴酸,氢溴酸是酸性物质,能使石蕊试液变红色;氢溴酸能和硝酸银反应生成淡黄色沉淀溴化银,所以观察D和E两试管,看到的现象是D中石蕊变红色,E管中出现浅黄色沉淀,
故答案为:D中石蕊变红色;E管中出现浅黄色沉淀;
(3)溴苯中 溴易挥发,溴和四氯化碳都是非极性分子,根据相似相溶原理知,溴易溶于四氯化碳,苯也易溶于四氯化碳,所以四氯化碳的作用是吸收溴化氢中的溴和挥发的有机物蒸汽,
故答案为:吸收溴化氢中的溴和挥发的有机物蒸汽;
(4)当两端压力发生压力变化时,液体会产生倒吸现象,DE装置中导气管不插入溶液中可以防止倒吸,倒置的漏斗下口很大,液体上升很小的高度就有很大的体积,上升的液体的本身的压力即可低偿压力的不均衡.因此由于上部还有空气隔离,液体不会倒吸入上端的细管道,所以具有防倒吸作用的仪器有DEF,
故答案为:DEF;
(5)苯与液溴发生取代反应生成溴苯和溴化氢,溴苯是密度大于水,无色的油状液体,溴化氢易挥发,能与水蒸气结合成氢溴酸液滴,溴化铁与氢氧化钠反应生成红褐色的氢氧化铁沉淀,
故答案为:溶液中有红褐色的絮状物生成,底部有无色油状物质生成,液面上有白雾;
(6)改进后的实验除①步骤简单,操作方便,成功率高;②各步现象明显;③对产品便于观察这三个优点外,还有一个优点是:对尾气进行处理,防止对空气造成污染,故答案为:对尾气进行处理,防止对空气造成污染.
点评 本题考查了苯的取代反应实验,考查的知识点有反应方程式的书写、产物的判断、蒸汽的成分及性质,综合性较强,为高频考点,题目难度中等,注意苯能和液溴发生取代反应,和溴水不反应.


 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ①④⑥ | C. | ②③⑤ | D. | ③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在2mL10%的氢氧化钠溶液中滴入2%的硫酸铜溶液4~6滴,配制新制氢氧化铜悬浊液,检验醛基 | |
| B. | 实验室制用乙醇与浓硫酸制乙烯时,迅速升温到140℃ | |
| C. | 盛放过苯酚的试剂瓶中残留的苯酚,用水洗涤 | |
| D. | 取加热至亮棕色的纤维素水解液少许,滴入新制的氢氧化铜悬浊液加热,证明水解产物为葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠原子失电子能力比镁弱 | B. | 水比硫化氢稳定 | ||
| C. | 硅酸比磷酸酸性强 | D. | 氢氧化钙比氢氧化锶碱性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲同学说:该条件下NaHCO3的溶解度较小 | |
| B. | 乙同学说:NaHCO3不是纯碱 | |
| C. | 丙同学説:析出NaHCO3固体后的溶液中只含氯化铵和氯化钠 | |
| D. | 丁同学说:从该反应可以获得氮肥 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A和B的转化率均是20% | B. | x=4 | ||
| C. | 平衡时A的物质的量为3.2mol | D. | 平衡时气体压强比原来减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
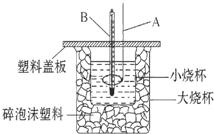 已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1.回答有关中和反应的问题.
已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1.回答有关中和反应的问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com