
| A、等质量的两种盐分别与足量盐酸反应,碳酸钠产生的气体多 |
| B、等质量的两种盐分别与足量盐酸反应,碳酸钠反应更剧烈 |
| C、盐酸滴加到碳酸钠溶液中与碳酸钠溶液滴加到盐酸中,两者的现象相同 |
| D、盐酸滴加到碳酸氢钠溶液中与碳酸氢钠溶液滴加到盐酸中,两者的现象相同 |
| m |
| M |
| 106 |
| 84 |
| 106 |
| 84 |


科目:高中化学 来源: 题型:
| A、0.1 mol?L-1的Na2CO3溶液中离子浓度关系:c (Na+)=2c (CO32-)+c (HCO3-)+c (H2CO3) |
| B、0.1 mol?L-1的NH4Cl和0.1 mol?L-1的NH3?H2O等体积混合后溶液中的离子浓度关系:c (Cl-)>c (NH4+)>c (H+)>c (OH-) |
| C、常温下,醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合溶液中,离子浓度关系:c (Na+)>c (CH3COO-) |
| D、0.1 mol?L-1的NaHS溶液中离子浓度关系:c (OH-)=c (H+)-c (S2-)+c (H2S) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7:Ba2++OH-+H++SO42-→BaSO4↓+H2O |
| B、将少量SO2气体通入NaClO溶液中:SO2+2ClO-+H2O→SO32-+2HClO |
| C、硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:2Fe2++2H++H2O2→2 Fe3++2H2O |
| D、向NaHCO3 溶液中加入过量Ca(OH)2 溶液:2HCO3-+Ca2++2OH-→2H2O+CaCO3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
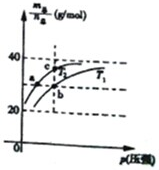 已知N2O4(g)?2NO2(g)△H>0且平衡体系的总质量(m总)与总物质的量(n总)之比在不同温度下随压强变化曲线如图所示,下列说法正确的是( )
已知N2O4(g)?2NO2(g)△H>0且平衡体系的总质量(m总)与总物质的量(n总)之比在不同温度下随压强变化曲线如图所示,下列说法正确的是( )| A、平衡常数K(a)=K(b)<K(c) | ||
| B、反应速率:va<vb | ||
| C、温度:T2>T1 | ||
D、当
|
查看答案和解析>>
科目:高中化学 来源: 题型:
A、vA=
| ||
B、vB=
| ||
| C、vC=4vB | ||
D、vD=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、54Fe和56Fe互为同位素 |
| B、质子数等于电子数的某微粒,可能是一种分子或离子 |
| C、只有一种分子组成的一定为纯净物 |
| D、16gO2和16gO3含有的原子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④ | B、①②④⑥ |
| C、①② | D、①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 实验 | 现象 | 结论 |
| A | 左边烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 | 活动性:Al>Fe>Cu |
| B | 左边棉花变橙色,右边棉花变蓝色 | 氧化性:Cl2>Br2>I2 |
| C | 白色固体先变为浅黄色,后变为黑色 | 溶解性:AgCl<AgBr<Ag2S |
| D | 锥形瓶中有气体产生,烧杯中溶液变浑浊 | 酸性:盐酸>碳酸>硅酸 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com