
| A. | Mg2+、NO3-、K+、Cl- | B. | Fe2+、NO3-、Al3+、Cl- | ||
| C. | Mg2+、SO42-、Na+、HCO3- | D. | K+、NH4+、AlO2-、SO42- |
分析 由水电离产生的c(H+)和 c(OH-)满足c(H+)•c(OH-)=10-24,c水(H+)=10-12,为酸或碱溶液,根据离子之间不能结合生成水、气体、沉淀、弱电解质等,则离子能大量共存,以此来解答.
解答 解:由水电离产生的c(H+)和 c(OH-)满足c(H+)•c(OH-)=10-24,c水(H+)=10-12,为酸或碱溶液,
A.Mg2+、NO3-、K+、Cl-之间不发生反应,都不与氢离子反应,在酸性溶液中能够大量共存,故A正确;
B.亚铁离子、铝离子与氢氧根离子反应,酸性条件下硝酸根离子氧化亚铁离子,在溶液中一定不能大量共存,故B错误;
C.碳酸氢根离子与氢离子、氢氧根离子反应,在溶液中一定不能大量共存,故C错误;
D.铵根离子与氢氧根离子反应,偏铝酸根离子与氢离子反应,在溶液中一定不能大量共存,故D错误;
故选A.
点评 本题考查离子的共存,为高考常见题型,侧重信息的提取和应用,把握离子之间的反应及影响水电离的因素即可解答,氧化还原为解答的难点,题目难度不大.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 原子与原子,链节跟链节均以共价键结合 | |
| B. | 原子与原子以共价键结合,链节跟链节以分子间作用力结合 | |
| C. | 原子跟原子、链节跟链节均以非极性共价键结合 | |
| D. | 原子跟原子以非极性共价键结合,链节跟链节以极性共价键结合 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 | |
| B. | 将废弃的秸秆转化为清洁高效的能源 | |
| C. | 为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 | |
| D. | 采用新技术开采煤、石油和天然气,以满足经济发展的需要 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3个 | B. | 4个 | C. | 5个 | D. | 6个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
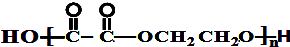 ,可由有机化工原料R和其它有机试剂,通过加成、水解、氧化、缩聚反应得到,则R是( )
,可由有机化工原料R和其它有机试剂,通过加成、水解、氧化、缩聚反应得到,则R是( )| A. | 1-丁烯 | B. | 乙烯 | C. | 1,3-丁二烯 | D. | 2-丁烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com