
【题目】【化学―选修5:有机化学基础】
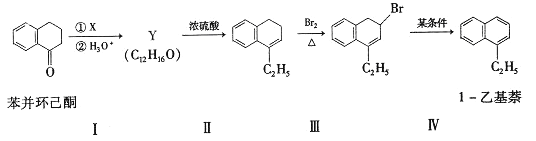
苯并环己酮是合成萘(![]() )或萘的取代物的中间体。由苯并环己酮合成1-乙基萘的一种路线如下图所示:
)或萘的取代物的中间体。由苯并环己酮合成1-乙基萘的一种路线如下图所示:
己知: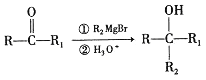
回答下列问题:
(l)萘的分子式为_______;苯并环己酮所含官能团是_______(填名称)。
(2)Y的结构简式为_________。
(3)步骤Ⅲ的反应属于_________(填反应类型)。
(4)步骤Ⅳ反应的化学方程式为____________(标明反应条件)。
(5)苯并环己酮用强氧化剂氧化可生成邻苯二甲酸。邻苯二甲酸和乙二醇经缩聚反应生成的高分子化合物的结构简式是________。
(6)1-乙基萘的同分异构体中,属于萘的取代物的有_______种(不含1-乙基萘)。W也是1 -乙基萘的同分异构体,它是含一种官能团的苯的取代物,核磁共振氢谱显示W有三种不同化学环境的氢原子,且个数比为1:1:2,W的结构简式为_________。
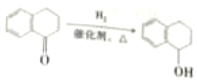
(7)仍以苯并环己酮为原料,上述合成路线中,只要改变其中一个步骤的反应条件和试剂,便可合成萘。完成该步骤:__________(表示方法示例:A ![]() B)。
B)。
【答案】 C10H8 羰基(或酮羰基) 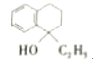 取代反应;(1分)
取代反应;(1分) 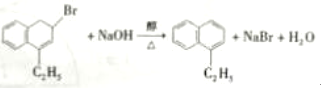
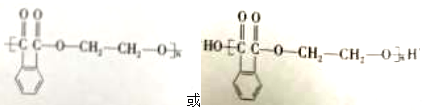 ; 11
; 11 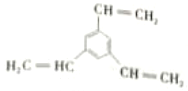 ;
; 
【解析】(l)根据萘的结构简式可知分子式为C10H8;苯并环己酮所含官能团是羰基。(2)Y在浓硫酸的作用下发生消去反应生成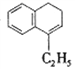 ,所以Y的结构简式为
,所以Y的结构简式为 。(3)步骤Ⅲ是氢原子被溴原子取代,属于取代反应。(4)步骤Ⅳ是溴原子发生消去反应生成1-乙基萘,因此生成反应的化学方程式为
。(3)步骤Ⅲ是氢原子被溴原子取代,属于取代反应。(4)步骤Ⅳ是溴原子发生消去反应生成1-乙基萘,因此生成反应的化学方程式为 。(5)邻苯二甲酸和乙二醇经缩聚反应生成的高分子化合物的结构简式是
。(5)邻苯二甲酸和乙二醇经缩聚反应生成的高分子化合物的结构简式是 。(6)1-乙基萘的同分异构体中,属于萘的取代物,如果含有1个取代基,只有一种;如果含有两个取代基,应该是2个甲基,有10种,共计有11种(不含1-乙基萘)。W也是1 -乙基萘的同分异构体,它是含一种官能团的苯的取代物,应该是碳碳双键或碳碳三键。核磁共振氢谱显示W有三种不同化学环境的氢原子,且个数比为1:1:2,因此含有的官能团只能是碳碳双键,则W的结构简式为
。(6)1-乙基萘的同分异构体中,属于萘的取代物,如果含有1个取代基,只有一种;如果含有两个取代基,应该是2个甲基,有10种,共计有11种(不含1-乙基萘)。W也是1 -乙基萘的同分异构体,它是含一种官能团的苯的取代物,应该是碳碳双键或碳碳三键。核磁共振氢谱显示W有三种不同化学环境的氢原子,且个数比为1:1:2,因此含有的官能团只能是碳碳双键,则W的结构简式为 。(7)将羰基直接加成转化为醇羟基,醇羟基发生消去反应即可转化为碳碳双键,因此该步骤
。(7)将羰基直接加成转化为醇羟基,醇羟基发生消去反应即可转化为碳碳双键,因此该步骤 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】每年的6月26日是国际禁毒日,珍爱生命,远离毒品。以下是四种毒品的结构简式,下列有关说法正确的是
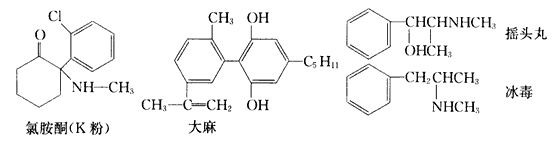
A. 四种毒品中都含有苯环,都属于芳香烃
B. 氯胺酮分子中所有碳原子可能共平面
C. 1 mol大麻与溴水反应最多消耗3molBr2
D. 摇头丸经过消去反应可制取冰毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数递增的4种短周期元素,其中Y、Z为金属元素。X、Y、Z、W的最高价氧化物对应的水化物甲、乙、丙、丁之间存在如右下图所示反应关系吸图中“—”相连的两种物质能发生反应)。下列判断一定正确的是

A. X是元素周期表中非金属性最强的元素 B. Z位于元素周期表第3周期IA族
C. 4种原子中,Y原子半径最大 D. W的最高化合价为+7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化钴(CoCl2)可溶于水,常用作湿度和水分的指示剂,工业上也可用于制取钴。
(1)钴元素的常见化合价与铁元素相同。往CoCl2溶液中加入NaOH溶液产生粉红色沉淀,露置于空气中一段时间后,沉淀变为棕褐色。
① 化合态钴的常见化合价有_______。
② 沉淀由粉红色变为棕褐色反应的化学方程式为_______________。
(2)将CoCl2溶于浓盐酸中能形成[CoCl4]2-,溶液中存在平衡:[Co(H2O)6]2++4Cl-![]() [CoCl2]2-+6H2O
[CoCl2]2-+6H2O
T1℃时,将0.025mol CoCl2·6H2O溶于50mL 12mol/L浓盐酸中,再加水稀释至100 mL。溶液中c(Cl-)与温度(T)的关系如右图所示。

① Tl ℃时,取10mL上述溶液稀释至l00mL,稀释后的溶液中c(Cl-)______0.6mol·L-1(填“>”“=”或“<”)。
② 由图可知,上述反应的△H______0(填“>”“=”或“<”)。
③ 根据A点数据,计算出T1℃时上述反应的平衡常数为________。
(3)采用下图所示装置(Ti-Ru电极为惰性电极)电解CoCl2溶液制取钴。Co能与强酸反应产生H2,不利于Co的沉积,故电解过程中,CoCl2溶液的pH通常控制在3.9~4.2。

① Co沉积在_______(填“Ti-Ru”或“Ti”) 电极上。
② CoCl2溶液中常含有少量Cu2+、Fe3+、Na+等,为提高产品的纯度和电流效率,电解前必须将其中的_______(填离子符号)除去。
③ 若用CoSO4溶液代替CoCl2溶液,会使产率降低。其原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对①100 mL 0.1 mol/L NaHCO3,②100mL 0.1 mol/L Na2CO3两溶液叙述正确的是( )
A.两溶液中c(OH--):①>②
B.两溶液中阳离子数目:②是①的2倍
C.②溶液中:c(HCO3--)<c(H2CO3)
D.①溶液中:c(CO32-)<c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度时,向2.0 L恒容密闭容器中充入2 mol SO2和1 mol O2,发生反应:
2SO2(g)+O2(g) ![]() 2SO3(g)。经过一段时间后达到平衡。反应过程中测定部分数据见下表:
2SO3(g)。经过一段时间后达到平衡。反应过程中测定部分数据见下表:
t / s | 0 | 2 | 4 | 6 | 8 |
n(SO3) / mol | 0 | 0. 8 | 1. 4 | 1.8 | 1.8 |
下列说法正确的是
A. 反应在前2 s 的平均速率v(O2) = 0. 4 mol·L-1·s-1
B. 保持其他条件不变,体积压缩到1.0 L,平衡常数将增大
C. 保持温度不变,向该容器中再充入2 mol SO2、1 mol O2,反应达到新平衡时n(SO3)/n(O2)增大
D. 相同温度下,起始时向容器中充入4 mol SO3,达到平衡时,SO3的转化率大于10%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,实验式相同,但既不是同系物,又不是同分异构体的是( )
A. 丙烯和丙烷 B. 正戊烷和2—甲基丁烷
C. 环己烷和苯 D. 乙炔和苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
(1)恒温恒容下,在某密闭容器中充入CO(NH2)2和H2O,在120℃、催化剂作用下发生反应:CO(NH2)2 (s) + H2O(g)![]() 2 NH3(g)+CO2(g) △H >0。
2 NH3(g)+CO2(g) △H >0。
关于该反应的下列说法正确的是____。
A.混合气体的平均相对分子质量不再改变,可以作为化学平衡到达的标志
B.在平衡体系中充入He可使H2O的体积分数增大
C.降低温度使CO(NH2)2的转化率增大
D.达到平衡后,再充入少量CO(NH2)2, H2O的转化率不变
(2)一定条件下,某密闭容器中充入等物质的量的NH3和CO2,发生反应:CO2(g) +2NH3(g)![]() CO (NH2)2 (s) +H2O(g),混合气体中NH3的体积分数[φ(NH3)]随时间变化关系如图所示。
CO (NH2)2 (s) +H2O(g),混合气体中NH3的体积分数[φ(NH3)]随时间变化关系如图所示。

则a点的正反应速率V正(CO2)____ b点的逆反应速率V逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com