
【题目】某温度下,将氯气通入氢氧化钾溶液中,反应后得到氯化钾,次氯酸钾,氯酸钾的混合溶液,经测定ClO与ClO3离子的物质的量的浓度之比为1:2,则氯气与氢氧化钾反应时,被还原的氯原子与被氧化的氯原子的物质的量之比为( )
A. 10:3B. 11:3C. 2:3D. 4:3
【答案】B
【解析】
Cl2生成ClO-、ClO3-化合价升高,是被氧化的过程,而Cl2生成NaCl是化合价降低被还原的过程,氧化还原反应中氧化剂和还原剂之间得失电子数目相等,根据ClO-与ClO3-的物质的量浓度之比可计算出失去电子的总物质的量,进而可计算得到电子的总物质的量;再根据氯元素被还原生成KCl的化合价变化为1,计算出被还原的氯原子的物质的量,最后计算出被还原的氯原子和被氧化的氯原子的物质的量之比.
Cl2生成ClO-与ClO3-是被氧化的过程,化合价分别由0价升高为+1价和+5价,CIO-与CIO3-的物质的量浓度之比为1:2,则可设ClO-为1mol,ClO3-为2mol,被氧化的氯元素共为3mol,失去电子的总物质的量为1mol×(1-0)+2mol×(5-0)=11mol,氧化还原反应中氧化剂和还原剂之间得失电子数目相等,Cl2生成KCl是被还原的过程,化合价由0价降低为-1价,则得到电子的物质的量也应为11mol,则被还原的Cl的物质的量为![]() ,所以被还原的氯原子和被氧化的氯原子的物质的量之比为11mol:3mol=11:3.
,所以被还原的氯原子和被氧化的氯原子的物质的量之比为11mol:3mol=11:3.
故本题选B。


 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案科目:高中化学 来源: 题型:
【题目】CO2 和 CH4 重整可制备合成气,催化重整反应历程示意图如下:
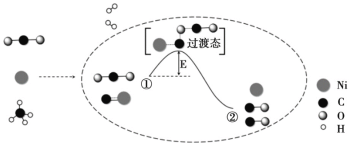
下列说法不正确的是
A.Ni 在该反应中做催化剂,参与化学反应
B.①→②吸收能量
C.①→②既有碳氧键的断裂,又有碳氧键的形成
D.合成气的主要成分为 CO 和 H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置测定镁带样品中单质镁的质量分数。(杂质与酸反应不产生气体)
完成下列填空:
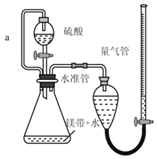
(1)硫酸必须过量的目的是_____
(2)导管a的作用是_____
(3)取两份镁带样品分别进行实验,所得数据见下表:
实验次数 | 镁带质量(g) | 氢气体积(mL)(已换算成标准状况) |
1 | 0.053 | 44.60 |
2 | 0.056 | 47.05 |
单质镁的质量分数是_____。(保留3位小数)
(4)如果测定结果偏高,可能的原因是_____。(选填编号)
a.装置漏气
b.未冷却至室温即读数
c.镁带中含有氧化镁
d.末读数时量气管的液面低于水准管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究电化学腐蚀及防护的装置如右图所示。下列有关说法错误的是( )

A. d为石墨,铁片腐蚀加快
B. d为石墨,石墨上电极反应为:O2 + 2H2O + 4e == 4OH–
C. d为锌块,铁片不易被腐蚀
D. d为锌块,铁片上电极反应为:2H+ + 2e == H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用碳酸钠晶体配制1.00mol/L的Na2CO3溶液100mL,造成所配溶液浓度偏高的原因是( )
A. 烧杯和玻璃棒没有洗涤
B. 向容量瓶转移液体时,容量瓶事先用蒸馏水洗涤
C. 定容时俯视刻度线
D. 称量碳酸钠晶体(Na2CO310H2O)的烧杯未干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮及其化合物的性质及转化,对研究自然界中氮的循环有着重大的意义。
I.合成氨反应历程研究
(1)科学家研究利用铁触媒合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示。
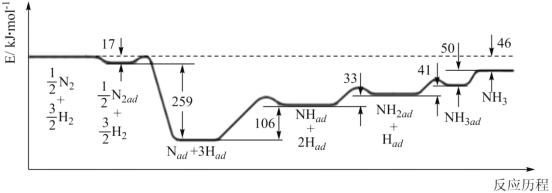
由图可知合成氨反应N2(g)+3H2(g)![]() 2NH3(g)的H=__kJ·mol-1。该历程中速率最慢的一步的化学方程式为__。
2NH3(g)的H=__kJ·mol-1。该历程中速率最慢的一步的化学方程式为__。
II.对NO与O2反应的研究
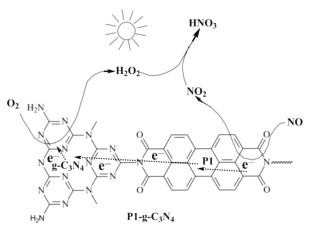
(2)用Pl-g-C3N4光催化氧化法脱除NO的过程如图所示。在酸性水溶液中,光催化脱除原理和电化学反应原理类似。g-C3N4端的反应为O2+2H++2e-=H2O2,则Pl端的反应为__。
(3)在一定条件下,将2molNO和1molO2通入恒容密闭容器中进行反应。在不同温度下,测得平衡时体系中NO、O2、NO2的物质的量与温度的关系如图所示。
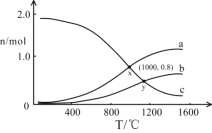
(已知:容器中发生两个反应2NO(g)+O2(g)![]() 2NO2(g) H0和2NO2(g)
2NO2(g) H0和2NO2(g)![]() N2O4(g) H0)
N2O4(g) H0)
①曲线c代表__的物质的量与温度的关系,x点对应的O2的转化率为__。
②下列说法正确的是__。
A.2NO+O2![]() 2NO2的平衡常数:x点>y点
2NO2的平衡常数:x点>y点
B.y点时2NO+O2![]() 2NO2的反应速率:v正<v逆
2NO2的反应速率:v正<v逆
C.x点对应的NO的物质的量分数为![]()
D.400~1200℃时,随温度升高,N2O4体积分数不断增大
III.对NO与Cl2物反应及产物NOCl(亚硝酰氯)的研究
(4)NOCl可由NO与Cl2制得,化学方程式为2NO(g)+Cl2(g)![]() 2NOCl ΔH=-111kJ/mol。在295K时,其反应物浓度与反应速率关系的数据如下:
2NOCl ΔH=-111kJ/mol。在295K时,其反应物浓度与反应速率关系的数据如下:
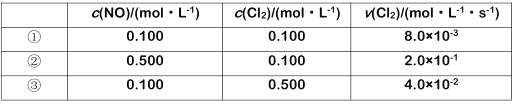
反应物浓度与反应速率关系式为v(Cl2)=k·cm(NO)cn(Cl2),式中速率常数k=Ae-Ea/RT,其中Ea为活化能,A、R均为大于0的常数,T为温度)。则此条件下k的数值为__,若要使k增大,可采取的措施有__、__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合I是一种重要的药物中间体,利用Robinson成环反应合成I的路线如图,回答下列问题:

已知:a.CH3COOCH3+CH3COOCH3![]()
b.
(1)A是一种环烃,且只有一种化学环境的H,则A的结构简式为__,C化学名称为__。
(2)C到D、F到G的反应类型分别为__、__。
(3)D到E的化学方程式为__。
(4)H所含官能团的名称为__,I的结构简式为__。
(5)G有多种同分异构体,满足下列条件的共有__种(不考虑立体异构),其中核磁共振氢谱有4组峰的结构简式为__(任写一种)。
①苯环上有4个取代基。②1molG可消耗3molNaOH。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的特殊情况。下列反应中属于这种情况的是( )
①过量的Zn与18 mol·L-1硫酸溶液反应 ②过量的氢气与少量的氮气在催化剂存在和一定条件下充分反应 ③过量的二氧化锰与浓盐酸 ④过量的铜与浓硫酸 ⑤过量的铜与稀硝酸 ⑥ 过量的稀硫酸与块状石灰石 ⑦常温下过量浓硫酸与铝
A.②③⑤B.②③④⑥⑦
C.①④⑤D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素推断题。
根据部分短周期元素的信息回答问题。
元素 | 元素信息 |
A | 第三周期VIIA族 |
B | 族序数是周期数的3倍 |
C | 原子序数是11 |
D | D3+与Ne的电子数相同 |
(1)A、B的元素符号分别为_______、________,C、D的元素名称分别为________、_______。B、D两元素在周期表中所在的位置分别是________、____________。
(2)写出B、C的单质在加热时的反应方程式:_____________。
(3)从原子结构的角度分析,C原子与D原子的__________相同。写出A的单质与水反应的离子方程式_______________,D的单质与C的氧化物的水化物溶液反应的化学方程式__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com