
【题目】设NA为阿伏加德罗常数的值,下列有关叙述正确的是 ( )
A.在标准状况下,22.4 L C2H6中含共价键的数目为6 NA
B.5 g KHCO3与CaCO3混合固体中阴离子数目为0.05 NA
C.常温下,1 L 0.1 mol·L–1 CH3COONa溶液中CH3COO-离子数目为0.1 NA
D.在Na2O2与H2O的反应中,当转移0.2 NA个电子时生成的O2体积为2.24 L
【答案】B
【解析】A.每个 C2H6分子中含有7个共价键,在标准状况下,22.4 L C2H6的物质的量为1mol,含共价键的数目为7 NA , A不符合题意;
B. KHCO3与CaCO3的相对分子质量均为100 g/mol,其组成结构中均含有一个阴离子,则5 g KHCO3与CaCO3混合固体中阴离子数目为0.05 NA , B符合题意;
C.CH3COONa溶液中CH3COO-要水解,其离子数目小于0.1 NA , C不符合题意;
D.没有指明气体所处的温度和压强,无法根据物质的量计算其体积,D不符合题意;
故答案为:B
A.根据公式![]() 计算气体的物质的量,结合 C2H6分子结构确定其共价键数;
计算气体的物质的量,结合 C2H6分子结构确定其共价键数;
B.混合的计算可采用极值法或平均法。二者的摩尔质量都是100 g/mol,则可采用平均法进行计算;
C.CH3COO-对应的酸为弱酸,在水中易发生水解;
D.未给出气体所处的状态,无法计算其体积;


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】作催熟剂的物质除乙烯外,还有氯酸镁。实验室制备少量氯酸镁晶体【Mg(ClO3)2·6H2O】的流程如下:
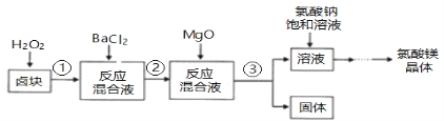

(1)步骤③的操作名称是___________,该步分离出的固体中含有多种成分,任写出一种成分的化学式__________________。
(2)用双氧水溶解卤块,H2O2的主要作用是_______________________
(3)加入饱和氯酸钠溶液发生的主要反应的反应类型是_________________(填四大基本反应类型)。
(4)若用10L饱和氯酸钠溶液(其中溶质利用率为90%),理论上可以制得氯酸镁晶体的质量是____________(用带a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到目的是( )
A.用NaHCO3溶液鉴别乙醇、乙酸和苯
B.苯和浓溴水混合,加入铁作催化剂制溴苯
C.裂化汽油可用作萃取剂来萃取溴水中的溴
D.除去乙烷中的乙烯,将混合气体通过盛有酸性KMnO4溶液的洗气瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证Cl2、Fe3+、I2三者氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器己略去,气密性已检验)。
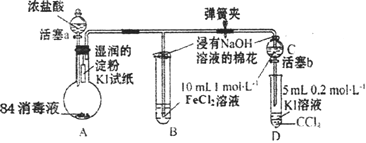
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.向B中加入一定量KSCN溶液,混合液显红色,一段时间后,B中溶液红色加深,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,写出A中发生反应的离子方程式________。
(2)验证氯气的氧化性强于碘单质的实验现象是________。
(3)B中溶液发生反应的离子方程式是________。
(4)为验证Fe3+的氧化性强于碘单质,过程Ⅳ的操作和现象是________,对应反应的离子方程式是________。
(5)浸有氢氧化钠溶液的棉花作用是________。
(6)过程Ⅲ实验的目的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向溴化钾、碘化钾的混合溶液中通入足量的氯气,再加热将溶液蒸干并灼烧,最后残留的物质是( )
A.KClB.KCl、I2C.KCl、KBrD.KCl、Br2、I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质既能发生消去反应生成相应的烯烃,又能氧化成相应的醛的是( )
A.CH3OH
B.CH2OHCH2CH3
C.(CH3)2COHCH3
D.(CH3)3COH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酿造厂生产的“老谢琼醋”是一种优质琼醋。某高二年级研究性学习小组,运用酸碱中和滴定的原理对“老谢琼醋”进行了定量分析,以测定其中的酸(全部以醋酸CH3COOH计)的含量:用酸式滴定管取10.00 mL这种琼醋,置于已知质量的小烧杯中称得其质量为12.5 g,再用100 mL容量瓶稀释至100 mL,滴定时每次取20.00 mL于锥形瓶中,而选用的标准溶液是0.112 5 mol/L NaOH溶液,以及合适的指示剂。读取的数据记录如下,其中第3次滴定的读数请从下图中读取。
滴定次数 | 用去NaOH溶液的体积 | ||
滴定前刻度 | 滴定后刻度 | 体积(mL) | |
1 | 3.20 | 22.48 | |
2 | 1.23 | 20.55 | |
3 | — | — | |
(1)请把有关数据填入表中所有空格里。
(2)琼醋样品从取出、称量、稀释到取液过程中,下列仪器水洗后不应再用相应琼醋润洗的仪器是()
A.酸式滴定管
B.烧杯
C.100 mL容量瓶
D.锥形瓶
(3)滴定时在锥形瓶底垫一张白纸的作用。
(4)滴定操作时,左手应 , 观察滴定管里液面的高度时应注意。
(5)选用的合适指示剂是 , 变色情况是。
(6)计算稀释后容量瓶中醋酸的物质的量浓度。
(7)计算“老谢琼醋”中醋酸的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质,按化合物、单质、混合物的顺序排列的是( )
A. 烧碱、液态氧、碘酒 B. 生石灰、白磷、冰水混合物
C. 干冰、铁、氯化氢 D. 空气、氮气、胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强碱性溶液中含有的离子是K+、NH4+、Al3+、AlO2﹣、CO32﹣、SiO32﹣、Cl﹣中的某几种,现进行如下实验: ①取少量的溶液用硝酸酸化后,该溶液无沉淀生成;
②另取一定量原溶液,逐滴加入盐酸至过量,发生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变后产生一种气体,最后沉淀逐渐减少至消失.
③另取一定量的原溶液中加入5mL0.2mol/L盐酸时,沉淀会完全消失,加入足量的硝酸银溶液可得到沉淀0.187g.
下列说法中正确的是( )
A.该溶液中一定不含NH4+、Al3+、SiO32﹣、Cl﹣
B.该溶液中一定含有Al3+、CO32﹣、Cl﹣
C.Cl﹣可能含有
D.该溶液中一定含有AlO2﹣、CO32﹣、Cl﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com