
下图表示的是难溶氢氧化物在不同pH下的溶解度(S/mol·L-1),下列说法中正确的是
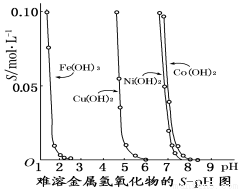
A.pH=3时溶液中铁元素的主要存在形式是Fe3+
B.若分离溶液中的Fe3+和Cu2+,可调节溶液的pH在4左右
C.若Ni(NO3)2溶液中含有少量的Co2+杂质,可通过调节溶液pH的方法来除去
D.若在含有Cu2+和Ni2+的溶液中加入烧碱,Ni(OH)2优先沉淀
科目:高中化学 来源:2015-2016学年江西省高一上学期期中考试化学试卷(解析版) 题型:选择题
用NA表示阿伏德罗常数,下列叙述正确的是
A.1.8g的NH4+离子中含有电子数11NA
B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
C.通常状况下,NA 个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5mol·L-1的MgCl2溶液中,含有Cl- 个数为1 NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上第三次月考化学试卷(解析版) 题型:填空题
Ⅰ、现有A g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示,则:
(1)该气体所含原子的个数为________________个。
(2)该气体在标准状况下的密度为_______________ g/L。
(3)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为________________mol/L。
Ⅱ、已知食盐常加人KIO3来补充碘元素,检验食盐中是否加碘,可利用如下反应:KIO3+5KI+3H2SO4 3K2SO4+3I2+3H2O
3K2SO4+3I2+3H2O
(1)如果反应中转移0.2mol电子,则生成I2的物质的量为 mol。
(2)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(气)+8NH3(气)=6NH4Cl(固)+N2(气)
若反应中消耗Cl2 1.5 mol,则被氧化的NH3在标准状况下的体积为______ L。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上第三次月考化学试卷(解析版) 题型:选择题
在某溶液中酚酞呈粉红色,下列离子在该溶液中不能大量存在的是
A.K+ B.Na+ C.Al3+ D.Ba2+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上第二次月考化学试卷(解析版) 题型:填空题
用惰性电极电解物质的量比为2:1的NaCl与NaHCO3混合溶液,测得溶液pH变化如右图所示。
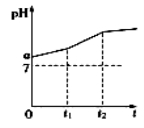
(1)在0→t1时间内,阳极上的电极反应式为:___________________________;
(2)用离子方程式表示:a点 pH﹥7原因:__________________________;0→t1时间内,溶液pH升高比较缓慢的原因:_______________________
(3)从原溶液中溶质变化角度看,t1时刻的意义是________________________
(4)有人利用电解原理开发出了一种家用“84”消毒液(有效成分为NaClO)发生器(构造如图),在制备该消毒液时,a电极应该连接在电源的________________极上,若两个电极一种是铁、一种是石墨,则b极材料是________________。

查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上第二次月考化学试卷(解析版) 题型:选择题
下列化学反应在理论上可设计成原电池是
A.2Al(s) + 2NaOH(aq) +2H2O(l) == 2NaAlO2(aq) + 3H2(g) △H<0
B.HNO3(aq) + KOH(aq) == KNO3(aq) + H2O(l) △H<0
C.Ba(OH)2·8H2O(s) + 2NH4Cl(s) == BaCl2(aq)+ 2NH3·H2O(aq)+ 8H2O(l) △H﹥0
D.Na2O(s)+ H2O(l) == 2NaOH(aq) △H<0
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上第二次月考化学试卷(解析版) 题型:选择题
常温下,将NH4NO3溶于水得无色溶液,为使该溶液中的c(NH4+)∶c(NO3-)=1∶1,可以采取的下列措施是
A.加入适量的HNO3,抑制NH4+水解 B.加入适量的氨水,使溶液的pH等于7
C.加入适量的NH4NO3(s) D.加入适量的NaOH,使溶液的pH等于7
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上第二次月考化学试卷(解析版) 题型:选择题
下列事实中不能用勒夏特列原理加以解释的是
A.压缩氢气与碘蒸气反应的平衡混合气体,颜色变深
B.浓氨水中加入氢氧化钠固体时产生较多的刺激性气味的气体
C.夏天,打开啤酒瓶时会在瓶口逸出气体
D.将盛有二氧化氮和四氧化二氮混合气的密闭容器置于冷水中,混合气体颜色变浅
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南宁远一中、祁阳一中高二上第二次联考化学试卷(解析版) 题型:填空题
已知NO2和N2O4可以相互转化:2NO2(g)  N2O4(g) ΔH<0。现将一定量NO2和N2O4的混合气体通入一体积为2 L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图。
N2O4(g) ΔH<0。现将一定量NO2和N2O4的混合气体通入一体积为2 L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图。

(1)图中共有两条曲线X和Y,其中曲线_______________表示NO2浓度随时间的变化;a、b、c、d四个点中,表示化学反应处于平衡状态的点是______________。
(2)①前10 min内用NO2表示的化学反应速率v(NO2)=__________mol·L-1·min-1。
②0~15 min ,反应2NO2(g)  N2O4(g)的平衡常数Kb=____
N2O4(g)的平衡常数Kb=____ ___________。
___________。
③25 min~35 min时,反应2NO2(g)  N2O4(g)的平衡常数Kd_____________Kb(填“>”、“=”或“<”)。
N2O4(g)的平衡常数Kd_____________Kb(填“>”、“=”或“<”)。
(3)反应25 min时,若只改变了某一个条件,使曲线发生如上 图所示的变化,该条件可能是_________________(用文字表达),若要达到使NO2(g)的百分含量与d点相同的化学平衡状态,在25 min时还可以采取的措施是_________________。
图所示的变化,该条件可能是_________________(用文字表达),若要达到使NO2(g)的百分含量与d点相同的化学平衡状态,在25 min时还可以采取的措施是_________________。
A.加入催化剂 B.缩小容器体积
C.升高温度 D.加入一定量的N2O4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com