
下列反应的离子方程式正确的是
A.氢氧化铜和盐酸反应:OH-+H+=H2O
B.钠和水反应:Na+2H2O=Na++2OH-+H2↑
C.铁和稀硝酸反应:Fe+2H+=Fe2++H2↑
D.常温下,NaOH溶液和Cl2反应:2OH-+Cl2=Cl-+ClO-+H2O
 计算高手系列答案
计算高手系列答案科目:高中化学 来源:2015届江西南昌三中高三11月份月考化学试卷(解析版) 题型:填空题
(10分)有A、B、C、D、E、F六种短周期元素,其元素特征信息如下表:

(1)写出两种均含A、B、C、F四种元素的化合物在溶液中相互反应的离子方程式
(2)D、E、F的简单离子半径由大到小的顺序是(直接用化学式表示) 。
(3)向Fe和D单质组成的混合物中,加入足量F的最高价氧化物对应水化物的稀溶液,固体全部溶解。向所得的溶液中加入过量的氢氧化钠溶液,将产生的沉淀过滤出来,经洗涤、干燥、灼烧后得到一种固体,经称量发现该固体的质量和原混合物的质量恰好相等。则原混合物中D单质的质量分数为 。
(4)一定量的石灰乳中通入一定量的E单质,两者恰好完全反应,生成物中有三种含E元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示。此时反应的化学方程式为 。
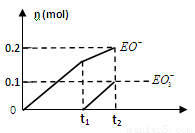
(5)A、B形成的化合物BA在有机合成中用途很广泛。它可以夺取很多化合物中的质子而生成相应的钠的化合物。写出它与乙醇反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市高三上学期期中考试化学试卷(解析版) 题型:填空题
(12分)Co2(OH)2CO3和Co(CH3COO)2·nH2O均是生产高比能锂电池正极材料的前驱体。
(1)这两种钴的化合物中钴的化合价为 。
(2)Co2(OH)2CO3在空气中充分加热生成四氧化三钴,该反应的化学方程式为 。
(3)为确定Co(CH3COO)2·nH2O中的n值及其热分解过程,取一定量的样品在氮气氛围中加热,样品的固体残留率( )随温度的变化如下图所示(样品在300℃前失去结晶水,图中A、B、C、D各处固体均为纯净物,其中C、D为氧化物)。
)随温度的变化如下图所示(样品在300℃前失去结晶水,图中A、B、C、D各处固体均为纯净物,其中C、D为氧化物)。
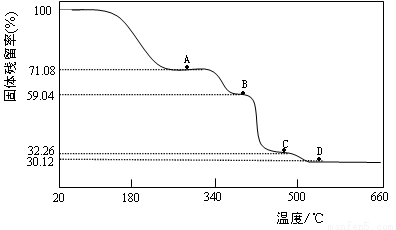
①Co(CH3COO)2·nH2O晶体中n= (填自然数)。
②A→B点反应释放的气体为纯净物(由两种元素组成),该气体的结构简式为 。
③B→C点反应释放CO、CO2两种气体,n(CO)∶n(CO2)= 。
④D点残留固体的化学式为 。(列出上述计算过程)
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市高三上学期期中考试化学试卷(解析版) 题型:选择题
最近美国化学家借助太阳能产生的电能和热能,用空气和水作原料成功地合成了氨气。下列有关说法正确的是
A.NH3是电解质
B.该合成氨过程不属于氮的固定
C.空气、水、太阳能均为可再生资源
D.断裂N2中的N≡N键会释放出能量
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市、建湖二中高二上期中化学试卷(必修)(解析版) 题型:选择题
关于反应2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O的说法正确的是
A.HCl是氧化剂
B.KMnO4在反应中被氧化
C.每生成1 mol Cl2转移2 mol e-
D.HCl仅表现出酸性
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市、建湖二中高二上期中化学试卷(必修)(解析版) 题型:选择题
环境污染已成为人类社会面临的重大威胁,下列对应关系不正确的是
| 环境问题 | 主要污染物 |
| 环境问题 | 主要污染物 |
A | 酸雨 | 二氧化硫 | C | 白色污染 | 二氧化硅 |
B | 温室效应 | 二氧化碳 | D | 光化学烟雾 | 二氧化氮 |
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市、建湖二中高二上期中化学试卷(必修)(解析版) 题型:选择题
配制500 mL 0.0500 mol·L-1的Na2CO3溶液,不需要的仪器有
A.500 mL容量瓶 B.锥形瓶 C.烧杯 D.玻璃棒
查看答案和解析>>
科目:高中化学 来源:2015届河南省高二上学期期中考试化学试卷(解析版) 题型:选择题
已知:C(s)+H2O (g)=CO(g)+H2(g) ΔH=akJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH= -220kJ·mol-1
H-H、O=O和O-H键的键能分别为436、496和462kJ·mol-1,则a为
A.-332 B.-118 C.+350 D.+130
查看答案和解析>>
科目:高中化学 来源:2015届河北省邯郸市高三上学期摸底考试化学试卷(带析版) 题型:填空题
(10分)进入2013年以来,我国中东部地区多次遭遇大范围、长时间的雾霾天气。车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”。
(1)活性炭可处理大气污染物NO。在2 L密闭容器中加入NO和活性炭(无杂质),生成气体E和F。当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
T/℃ n/mol
| 活性炭 | NO | E | F |
初始 | 2.030 | 0.10 | 0 | 0 |
T1 | 2.000 | 0.040 | 0.030 | 0.030 |
T2 | 2.005 | 0.050 | 0.025 | 0.025 |
①结合上表数据,写出NO与活性炭反应的化学方程式 。
②上述反应T1℃时的平衡常数K1= 。
③根据上述信息判断,温度T1和T2的关系是(填序号) 。
a.T1>T2 b.T1<T2 c.无法比较
(2)车辆排放的氮氧化物和碳氧化物在催化剂作用下可发生反应:2CO+2NO N2+2CO2 在一体积为1L的密闭容积中,加入0.40mol的CO和0.40mol的NO ,反应中N2的物质的量浓度的变化情况如图所示,回答下列问题。
N2+2CO2 在一体积为1L的密闭容积中,加入0.40mol的CO和0.40mol的NO ,反应中N2的物质的量浓度的变化情况如图所示,回答下列问题。
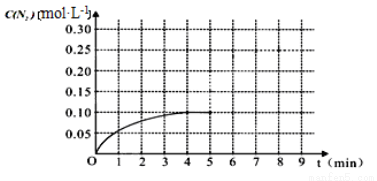
①计算从反应开始到平衡时,平均反应速率v(N2)= 。
②在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时N2的浓度约为0.25 mol·L-1)。请在上图中画出第5分钟末到此平衡时N2浓度的变化曲线。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com