
| 选项 | 实验操作设计 | 现象记录 | 结论解释 |
| A | 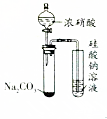 打开分液漏斗 | 右侧试管中出现白色沉淀 | 酸性:HNO3>H2CO3>H2SiO3 |
| B | 向稀硝酸和稀硫酸中分别加入铁粉 | 均有气泡冒出 | 两者均发生氧化还原反应 |
| C | 将SO2通入Ba(NO3)3溶液中 | 有白色沉淀生成 | 白色沉淀是BaSO3 |
| D | 向盛有Fe(NO3)3溶液的试管中加入0.1mol•LH2SO4溶液 | 试管口出现红棕色气体 | 溶液中NO3-被Fe2+ 还原为NO2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.硝酸具有挥发性,导致生成的二氧化碳中含有硝酸,硝酸能和硅酸钠反应生成难溶性的硅酸;
B.稀硝酸和Fe反应生成NO、稀硫酸和Fe反应生成氢气,两个反应都有电子转移;
C.二氧化硫和硝酸钡溶液发生氧化还原反应生成硫酸钡沉淀和NO;
D.酸性条件下,硝酸根离子具有强氧化性,能氧化亚铁离子生成铁离子,自身被还原生成NO.
解答 解:A.硝酸具有挥发性,导致生成的二氧化碳中含有硝酸,硝酸能和硅酸钠反应生成难溶性的硅酸,干扰二氧化碳和硅酸钠溶液反应,所以在将气体通入硅酸钠溶液之前除去硝酸,故A错误;
B.稀硝酸和Fe反应生成NO、稀硫酸和Fe反应生成氢气,两个反应都有电子转移,都是氧化还原反应,故B正确;
C.二氧化硫和硝酸钡溶液发生氧化还原反应生成硫酸钡沉淀和NO,所以得到的沉淀是硫酸钡而不是亚硫酸钡,故C错误;
D.酸性条件下,硝酸根离子具有强氧化性,能氧化亚铁离子生成铁离子,自身被还原生成NO,NO再和空气中氧气反应生成红棕色二氧化氮,故D错误;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及酸性强弱比较、氧化还原反应等知识点,明确实验原理、物质性质差异性是解本题关键,注意A中要排除硝酸的干扰,注意D中亚铁离子和硝酸的反应,为易错点.


科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某电中性单核粒子含有6个电子、7个中子,该粒子是${\;}_{6}^{13}$C | |
| B. | 在Na+、O2-、Cl、Cl-四种粒子中,半径最大的是Cl-,半径最小的是Na+ | |
| C. | 在离子RO3n-中共有x个核外电子,R原子的质量数为A,则R原子核内含有的中子数目是A-x+n+24 | |
| D. | 硫离子的结构示意图为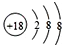 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所有的烷烃,彼此都是同系物 | |
| B. | 两种化合物的组成元素相同,各元素的质量分数也相同,二者一定具有相同最简式 | |
| C. | 组成元素的质量分数相同的不同化合物互为同分异构体 | |
| D. | 互为同系物的有机物相对分子质量一定相差14的整数倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 编号 | 实验操作 | 预期现象和结论 |
| ① | 取少量样品于试管中,加入适量蒸馏水溶解后,向试管中加入足量稀硝酸 | 有气体产生,说明样品中含有Na2CO3 |
| ② | 向试管中加入足量Ba(NO3)2溶液 | 若有沉淀产生,则含Na2SO4,若没有沉淀产生,则不含Na2SO4 |
| ③ | 若②操作无沉淀,则向试管中加入0.1mol•L-1AgNO3溶液.若②操作中有沉淀,则将试管静置片刻后,取上层清液于另一去试管中,加入0.1mol•L-1AgNO3溶液 | 有沉淀产生,则含NaCl;无沉淀产生,则不含NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冰的密度比液态水的密度小是因为冰分子之间含有较强的化学键 | |
| B. | 氨分子的键角比甲烷分子的键角小是因为两个分子中中心原子的杂化方式不同 | |
| C. | HF的沸点比HCl的沸点高是因为HF分子内含有氢键 | |
| D. | HF比HCl稳定是因为HF分子中共价键的键能大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com