
����Ŀ��ijʵ��С��̽��SO2��Cu(OH)2����Һ�ķ�Ӧ��
��1��ʵ��һ������ͼװ�ã��г�װ�����ԣ��������Ѽ��飩�Ʊ�SO2����SO2ͨ��Cu(OH)2����Һ�ķ�Ӧ�С�B�г���������ɫ�������Ժ�B��������Һ����ɫ����CuSO4��Һ��CuCl2��Һ����ɫ�����Բ�ͬ��
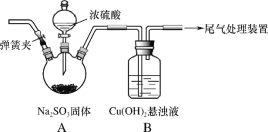
���ų�װ���еĿ�������������Է�Ӧ���ŵIJ�����_____���رյ��ɼС�
�ڴ�Һ©��������A�з�����Ӧ�ķ���ʽ��_____��
��2��ʵ�����Ϊȷ����ɫ����ɷ֣���������ʵ�飺
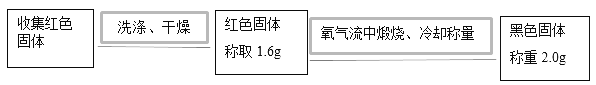
���������������պ�ɫ�����Ŀ����_____��
�ڸ�������ʵ��ɵý��ۣ��ú�ɫ����Ϊ_____��
��3��ʵ������Ϊ̽��B����Һ����ɫ��������ɫ��ԭ��ʵ�����£�
i.��4mL1mol/L��CuSO4��Һ��ͨ�����SO2��δ����Һ��ɫ�����仯��
ii.ȡ����B����Һ����������ϡ���ᣬ������ɫ�̼�����ζ�����壬�õ��������ɫ��Һ���ټ���BaCl2��Һ�����ְ�ɫ������
�������ϣ�SO2�����������»�ԭ�Խϲ
��ʵ��i��Ŀ��_____��
�ڸ�������ʵ��ɵý��ۣ���Һ����ɫ��ԭ������Һ�к��н϶�Cu(HSO3)2��С��ͬѧͨ����һ��ʵ��ȷ�������ֿ����ԣ�������1mol/L��CuSO4��Һ�м���_____��Һ���õ���ɫ��Һ��
��4������ʵ����Եó������ֺ�ɫ������ԭ���ǣ�_____���������ӷ���ʽ��ʾ����Һ������ɫ��ԭ���ǣ�_____�����û�ѧ����ʽ��ʾ��
���𰸡����ɼУ�ͨ��N2һ��ʱ�� H2SO4+Na2SO3=Na2SO4+SO2��+H2O ����ɫ����ת��Ϊ����ͭ Cu �ų��ܽ��SO2��H2SO3������Һ����ɫ�Ŀ����� NaHSO3��KHSO3 SO2+Cu(OH)2+2OH-=Cu+SO42-+2H2O 2SO2+Cu(OH)2=Cu(HSO3)2
��������
(1)��Ϊ�ų�������ʵ��ĸ��ţ��μ�Ũ����֮ǰӦ��ͨ�뵪�����������ų���
��װ��A�еķ�Ӧ���Ʊ�SO2�ķ�Ӧ��
(2)��SO2ͨ��Cu(OH)2����Һ�ķ�Ӧ�У�B�г���������ɫ�������п�����Cu��Cu2O����ߵĻ���
���������������պ�ɫ�����Ŀ���ǽ���ɫ����ת��Ϊ����ͭ�������ں��������жϣ�
����ʵ�������ʵ����������ɫ�����ƽ��Ħ��������������������ɷ֣�
(3)�ٸ���B��������Һ�п��ܵijɷֵȣ�ʵ��i�����ų����ֳɷ�����ɫ�Ŀ����ԣ�
��ȷ��Cu(HSO3)2ʹ��Һ����ɫ����Ҫ����Һ�м��뺬��HSO3-���ӵ����ʣ�
(4)���ֺ�ɫ������ԭ����������Cu����Һ������ɫ��ԭ�������˺�HSO3-���ӵ����ʡ�
(1)��Ϊ�ų�������ʵ��ĸ��ţ��μ�Ũ����֮ǰӦ��ͨ�뵪�����������ų�������Ϊ�����ɼУ�ͨ��N2һ��ʱ�䣬�رյ��ɼУ�
��װ��A�еķ�Ӧ���Ʊ�SO2�ķ�Ӧ����ѧ����ʽΪH2SO4+Na2SO3=Na2SO4+SO2��+H2O��
(2)��SO2ͨ��Cu(OH)2����Һ�ķ�Ӧ�У�B�г���������ɫ�������п�����Cu��Cu2O����ߵĻ���
���������������պ�ɫ�����Ŀ���ǽ���ɫ����ת��Ϊ����ͭ�������ں��������жϣ�
����ʵ���֪n(CuO)=![]() =0.025mol�����ɫ�����ƽ��Ħ������Ϊ
=0.025mol�����ɫ�����ƽ��Ħ������Ϊ![]() =64g/mol���ʺ�ɫ����Ϊͭ��
=64g/mol���ʺ�ɫ����Ϊͭ��
(3)��B��������Һ�п��ܺ����ܽ��SO2��H2SO3��Cu(HSO3)2��CuSO4�ȣ�CuSO4����Һ�г���ɫ����B ������Һ����ɫ��ʵ��i�����ų��ܽ��SO2��H2SO3������Һ����ɫ�Ŀ����ԣ�
��ȷ��Cu(HSO3)2ʹ��Һ����ɫ����Ҫ����Һ�м��뺬��HSO3-���ӵ����ʣ��ʿɼ���NaHSO3��KHSO3��
(4)���ֺ�ɫ������ԭ����������Cu�����ӷ���ʽΪ��SO2+Cu(OH)2+2OH-=Cu+SO42-+2H2O����Һ������ɫ��ԭ�������˺�HSO3-���ӵ����ʣ����ӷ���ʽΪ2SO2+Cu(OH)2=Cu(HSO3)2.


 ���������������Բ��������ϵ�д�
���������������Բ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ݹ������IJ�ͬ�������л�����з��ࡣ
��CH3CH2OH�� ��CH3CH2Br��
��CH3CH2Br��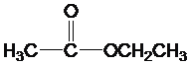 ��
��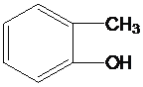 ��
��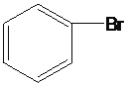 ��
��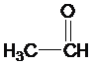 ��
��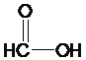 ��
��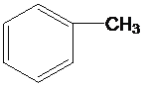 ��
��
(1)��������____________________________��
(2)±������_____________________________��
(3)����_________________________________��
(4)�ӣ�__________________________________��
(5)ȩ��____________________________________��
(6)ͪ��___________________________________��
(7)���_________________________________��
(8)����____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
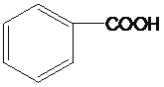
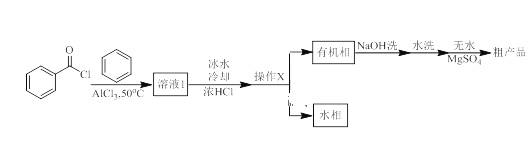
����Ŀ��������ͪ�㷺Ӧ����ҩ��ϳɣ�ͬʱҲ���л����ϡ�ɱ����ȵ���Ҫ�м��塣ʵ�����Ա��뱽������Ϊԭ�ϣ���AlCl3�������Ʊ�������ͪ��ʵ����������ͼ��ʾ��
������������������������±���
���� | ��Է� ������ | �ܶ�/g��cm-3 | �۵�/oC | �е�/oC | �ܽ��� |
�� | 78 | 0.88 | 5.5 | 80.1 | ����ˮ�������Ҵ� |
�������� | 140.5 | 1.22 | 1 | 197 | ��ˮ�ֽ� |
��ˮ�Ȼ��� | 133.5 | 2.44 | 190 | 178�������� | ��ˮˮ�⣬�ܱ� |
������ͪ | 182 | 1.11 | 48.5 | 305����ѹ�� | ����ˮ�����ܱ� |
��֪����Ӧԭ��Ϊ�� ���÷�Ӧ���ҷ��ȡ�
���÷�Ӧ���ҷ��ȡ�
�ش��������⣺
��1����Ӧװ����ͼ��ʾ�����Ⱥͼг�װ������ȥ����Ѹ�ٳ�ȡ7.5 g��ˮ���Ȼ�����������ƿ�У��ټ���30 mL��ˮ�������裬�����μ�6 mL��������ı������ȡ���ӦҺ����ɫ��Ϊ��ɫ�����Ȼ������ܽ⡣��������50�����ҷ�Ӧ1.5��2 h��
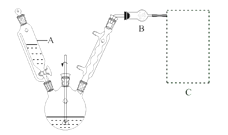
����A������Ϊ_______��װ��B������Ϊ_______�������μӱ������ȵ�ԭ����______������ΪC��װ�õ���_______�����ţ���
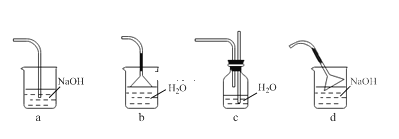
��2������XΪ___________��
��3��NaOH��Һϴ�ӵ�Ŀ����_____________��
��4���ֲ�Ʒ�Ⱦ���ѹ�����ȥ__________���ټ�ѹ����õ���Ʒ��
��5���������Ʒ�۵�Ϊ________ʱ��ȷ����ƷΪ��Ʒ����֪ʵ���������ô�Ʒ8.0 g����ʵ�����Ϊ_________ %��������λ��Ч���֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���20.00mL0.1000mol��L-1�Ĵ�����Һ����μ���0.1000mol��L-1��NaOH��Һ��pH��NaOH��Һ����ı仯��ͼ��ʾ������˵������ȷ���ǣ� ��
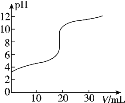
A.�ڵζ������У�c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
B.pH=5ʱ��c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
C.pH=7ʱ������NaOH��Һ�����С��20.00mL
D.�ڵζ������У���NaOH��Һ�μ�c(CH3COO-)��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ʒ��ҽҩ��Ⱦ�ϵȹ�ҵ���й㷺Ӧ�ã���ṹʽ��ͼ��ʾ������ˮ���ȩˮ��Һ����������Ƶ�������Ʒ����ԭ����ȫ��Ӧ����������Ʒ�������ȩ�����ʵ���֮��Ϊ�� ��

A.1��1B.2��1C.2��3D.3��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£������Ϊ3 L���ܱ������У�һ����̼��������Ӧ���ɼ״�(����ΪCu2O/ZnO)��CO(g)��2H2(g)CH3OH(g)��
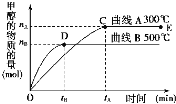
��������������и��⣺
(1)��Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������ʽK��__________�������¶ȣ�Kֵ__________(����������������С������������)��
(2)��500�棬�ӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v(H2)��______________��
(3)�������������������£��Դ���E�����ϵ���ѹ����ԭ����1/2�������йظ���ϵ��˵����ȷ����__________(����ĸ���)��
a.������Ũ�ȼ�С b.����Ӧ���ʼӿ죬�淴Ӧ����Ҳ�ӿ�
c.�״������ʵ������� d.����ƽ��ʱn(H2)/n(CH3OH)����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״�����Ҫ�Ļ���ԭ�ϡ����úϳ���(��Ҫ�ɷ�ΪCO��CO2��H2)�ڴ����������ºϳɼ״������ܷ����ķ�Ӧ���£�
i CO2(g)+ 3H2(g) ![]() CH3OH(g)+ H2O(g) H1=Q kJ��mol-1
CH3OH(g)+ H2O(g) H1=Q kJ��mol-1
ii. CO2(g)+ H2(g) ![]() CO(g)+H2O(g) H2=+41 kJ��mol-1
CO(g)+H2O(g) H2=+41 kJ��mol-1
iii. CO(g)+2H2(g) ![]() CH3OH(g) H3= 99 kJ��mol-1
CH3OH(g) H3= 99 kJ��mol-1
�ش��������⣺
��1��Q=_________
��2��ͼ������ȷ��ӳƽ�ⳣ��K3(��Ӧiii��ƽ�ⳣ��)���¶ȱ仯��ϵ������Ϊ__������ĸ��
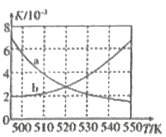
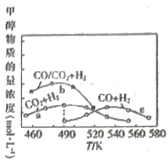
��3����ͼΪ��λʱ����CO2+H2��CO+ H2��CO/CO2+H2�������������ɼ״������ʵ���Ũ�����¶ȵĹ�ϵ(����������ͨ���CO��CO2��H2�����ʵ���Ũ����ͬ)��490Kʱ����������a��c�жϺϳɼ״�ʱ��Ҫ�����ķ�ӦΪ________(����i������iii��)��������a��֪���״�������������С����ԭ����_________________________________��
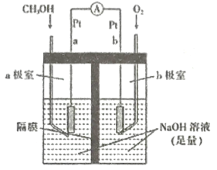
��4����ͼ����NaOH��ҺΪ�������Һ�ļ״�ȼ�ϵ��:�缫a�ķ�ӦʽΪ____________������ĤΪ�����ӽ���Ĥ����ÿת��6mol���ӣ���Һ����_______mol Na+��____________(����������������������")�ƶ���
��5��CO2��������Ҳ�������ɵ�̼������Ҫ������������Ӧ��
��ӦI:CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
��ӦII :2CO2(g)+6H2(g) ![]() C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)
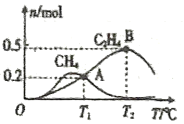
��1L�����ܱ������г���2molCO2��4molH2���ƽ��ʱ�й����ʵ����ʵ������¶ȱ仯��ͼ��ʾ��T1��ʱ,CO2��ת����Ϊ______��T1��ʱ����ӦI��ƽ�ⳣ��K=_________(������λ��Ч����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Լ��������ö������ױ���ԭ����һ�������Ƶá� ��Ҫ��Ӧ��װ������:
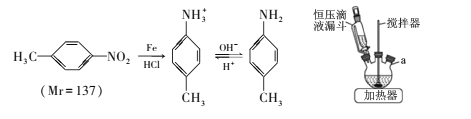
��Ҫ��Ӧ��Ͳ�����������ʼ��±�:
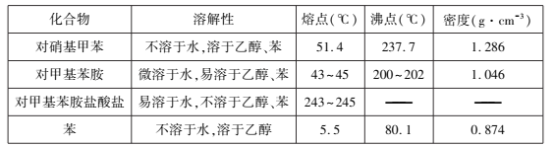
ʵ�鲽������:
����������ƿ�м���50mLϡ���ᡢ10.7mL(13.7g)�������ױ�����������,ά��ƿ���¶���80������,ͬʱ���������ʹ���ַ�Ӧ;
�ڵ���pH=7~8,����μ���30mL����ֻ��;
�۳��˵õ�����,����Һ���á���Һ��Һ��M;
����M�еμ�����,�����á���Һ,���²�Һ���м���NaOH��Һ,���������;
�ݳ��˵ù���,����ϴ�ӡ������6.1g��Ʒ��
�ش���������:
��1����Ҫ��Ӧװ������ͼ,a��ȱ�ٵ�װ����____ (����������),ʵ�鲽��ۺܵ͢ķ�Һ������ʹ�õ����������е�_____(����)��
a.�ձ��� b.©���� c.�������� d.����̨
��2�����������5%��̼������Һ��pH =7~8��Ŀ��֮һ��ʹFe3+ ת��Ϊ������������,��һ��Ŀ���ǡ�____��
��3���������Һ��M�Ƿ�Һʱ��____ ��(��ϡ����¡�)Һ��,���������������____��
��4��������м�������������Һ������Ӧ�����ӷ���ʽ��____��
��5���������,����ϴ�Ӽ�������ʵ���____ (����)��
a.�Ҵ��� b.����ˮ�� c.HCl��Һ�� d.NaOH��Һ
��6����ʵ��IJ�����_____%��(����������һλС��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ը�����������Ҫ�ɷ�ΪAl2O3��Fe2O3��SiO2������FeS2�ͽ��������Σ�Ϊԭ�ϣ����������������Fe3O4�IJ��ֹ����������£�

��1�����չ��̾������SO2����NaOH��Һ���չ���SO2�����ӷ���ʽΪ______________________��
��2������1%CaO�Ͳ�����CaO�Ŀ�۱��գ�����ȥ�������¶ȱ仯��������16ͼ��ʾ��

��֪���������������εķֽ��¶ȶ�����600 ��
��ȥ����=��1��![]() ����100%
����100%
�ٲ�����CaO�Ŀ���ڵ���500 �決��ʱ��ȥ������Ԫ����Ҫ��Դ��__________________��
��700�決��ʱ������1%CaO�Ŀ����ȥ���ʱȲ�����CaO�Ŀ����ȥ���ʵͣ�����Ҫԭ����______________________________________________________��
��3�������������õ�����Һ��ͨ�����CO2����Ԫ�ش��ڵ���ʽ��_______________���ѧʽ��ת��Ϊ_______________���ѧʽ����
��4�����������õ��������к�������Fe2O3��Fe2O3��FeS2��Ϻ���ȱ�������±�������Fe3O4��SO2����������ȫ��Ӧ���ĵ�n��FeS2����n��Fe2O3��=__________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com