
| A. | 甲烷和丙烯 | B. | 甲烷和丁烯 | C. | 乙烷和乙烯 | D. | 丙烷和乙烯 |
分析 在同温同压下,混合气体对氢气的相对密度为13,则该混合气体的平均相对分子质量为13×2=26,据此可判断该混合气体中一定含有甲烷;
标况下8.96L混合气体的物质的量为$\frac{8.96L}{22.4L/mol}$=0.4mol,则混合气体的总质量为0.4mol×26g/mol=10.4g,溴水质量增重5.6g为烯烃的质量,根据总质量可计算出甲烷的质量及物质的量,从而可知烯烃的物质的量,再根据M=$\frac{m}{n}$计算出该烯烃的摩尔质量,最后根据烯烃的通式CnH2n确定该烯烃即可.
故甲烷的质量为10.4g-5.6g=4.8g,故甲烷的物质的量为:$\frac{4.8g}{16g/mol}$=0.3mol,则烯烃的物质的量为:0.4mol-0.3mol=0.1mol,该烯烃的摩尔质量为:$\frac{5.6g}{0.1mol}$=56g/mol,设烯烃的组成为(CH2)n,则14n=56,解得:n=4,故该烯烃为丁烯.
解答 解:在同温同压下,混合气体对氢气的相对密度为13,故混合气体的平均相对分子质量为13×2=26,故一定含有甲烷;
标况下8.96L混合气体的物质的量为$\frac{8.96L}{22.4L/mol}$=0.4mol,故混合气体的总质量为0.4mol×26g/mol=10.4g,溴水质量增重5.6g为烯烃的质量,故甲烷的质量为10.4g-5.6g=4.8g,故甲烷的物质的量为:$\frac{4.8g}{16g/mol}$=0.3mol,则烯烃的物质的量为:0.4mol-0.3mol=0.1mol,该烯烃的摩尔质量为:$\frac{5.6g}{0.1mol}$=56g/mol,
设烯烃的分子式为CnH2n,则14n=56,解得:n=4,故该烯烃为丁烯,
所以该混合气体为甲烷和丁烯的混合物,
故选B.
点评 本题考查了混合物反应的计算,题目难度中等,明确常见有机物性质为解答关键,注意掌握相对密度与摩尔质量之间的关系,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测液体积/mL | 标准碘溶液体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 平均值 | ||
| 1 | 25.00 | 0.00 | 14.97 | ① |
| 2 | 25.00 | 0.10 | 15.13 | |
| 3 | 25.00 | 0.22 | 14.93 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两者水溶液均呈碱性,碳酸钠俗名纯碱,物质分类属于碱 | |
| B. | 两者均和稀盐酸反应产生CO2,但碳酸氢钠和盐酸反应更剧烈 | |
| C. | 用酒精灯加热时两者均可发生分解反应,但碳酸氢钠更易分解 | |
| D. | 两者均可和澄清石灰水发生反应,但碳酸氢钠反应时无沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,14.2克 Na2SO4含有的Na+离子数为0.2NA | |
| B. | 标准状况下,22.4LH2O含有的分子数为 NA | |
| C. | 通常状况下,NA个N2分子占有的体积为22.4L | |
| D. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
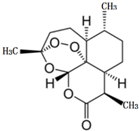 2015年10月,中国女药学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖.这是中国生物医学界迄今为止获得的世界级最高级大奖.青蒿素的键线式化学结构如图所示,下列说法不正确的是( )
2015年10月,中国女药学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖.这是中国生物医学界迄今为止获得的世界级最高级大奖.青蒿素的键线式化学结构如图所示,下列说法不正确的是( )| A. | 青蒿素属于芳香化合物,能与H2发生加成反应 | |
| B. | 青蒿素能与氢氧化钠溶液发生反应 | |
| C. | 青蒿素的化学式为C15H22O5 | |
| D. | 青蒿素的核磁共振谱图中有12个峰 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com