
| 催化剂 |
 ,
,| 催化剂 |
 ,加聚反应(或聚合反应);
,加聚反应(或聚合反应);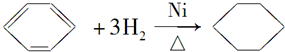 ,
,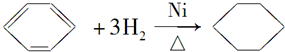 ;加成反应;
;加成反应; ,
, ,取代反应;
,取代反应;| 醇 |
| △ |
| 醇 |
| △ |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | NaOH | 偏向Mg |
| 5 | Al、Zn | 浓硝酸 | 偏向Al |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
A、 在如图所示NaCl晶体中,距Na+最近的Cl-形成正八面体 |
B、 在如图所示气态团簇分子的分子式为EF或FE |
C、 在如图所示CO2晶体中,一个CO2分子周围有12个CO2分子紧邻 |
D、 在如图所示碘晶体中,碘分子的排列有两种不同的方向 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com