
| A、HCN易溶于水 |
| B、HCN溶液能导电 |
| C、1mol/L氢氰酸溶液的pH约为3 |
| D、10 mL1 mol?L-1HCN恰好与10 mL 1 mol?L-1 NaOH溶液完全反应 |


科目:高中化学 来源: 题型:
A、水玻璃中通入足量的CO2:Si
| ||
| B、氯化亚铁溶液中通入足量的Cl2:2Fe2++Cl2═2Fe3++2Cl- | ||
| C、NaHCO3溶液中加入足量NaHSO4溶液:2H++CO32-═CO2↑+H2O | ||
| D、NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、③⑤ | C、④⑤ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某溶液做焰色反应,现象为黄色,说明该溶液中不存在K+ |
| B、配制950mL1mol/LNa2CO3溶液时,应用托盘天平称取100.7g无水Na2CO3 |
| C、为证明酸性H2CO3>H2SiO3,可将CO2气体通入Na2SiO3溶液中观察现象 |
| D、用酒精萃取碘水中的I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3c-a-b |
| B、a+b-3c |
| C、a+3b-2c |
| D、a+3b-6c |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某学生为验证苯的沸点(80.1℃)比水低,设计了如图1所示的实验装置:(某些固定装置已略去)
某学生为验证苯的沸点(80.1℃)比水低,设计了如图1所示的实验装置:(某些固定装置已略去)查看答案和解析>>
科目:高中化学 来源: 题型:
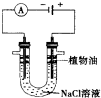 铁是一种过渡元素,金属铁是最常用的金属.请回答下列各题:
铁是一种过渡元素,金属铁是最常用的金属.请回答下列各题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com