
| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
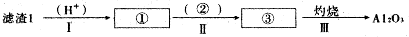
分析 分析流程锂辉石主要成分为Li2O•Al2O3•4SiO2,含有少量Ca、Mg元素,研磨在加热条件下用浓硫酸酸浸后过滤得到Li2SO4,硫酸镁和硫酸钙,滤渣Ⅰ为Al2O3•4SiO2•H2O↓,滤液加入为石灰乳是氢氧化钙,提供氢氧根离子和钙离子,加入碳酸钠沉淀钙离子,更完全的沉淀镁离子和碳酸根离子,过滤得到滤液主要是Li2SO4,加入饱和碳酸钠沉淀锂离子为碳酸锂,滤渣2主要成分有Mg(OH)2和CaCO3,
(1)从滤渣1中分离出Al2O3的流程分析,加入酸溶解Al2O3•4SiO2•H2O,得到硫酸铝溶液和二氧化硅,过滤得到溶液硫酸铝,加入氨水或适量氢氧化钠溶液得到氢氧化铝沉淀,灼烧得到氧化铝;步骤Ⅱ中铝离子与氨水反应生成氢氧化铝沉淀;
(2)滤渣2的主要成分有Mg(OH)2和CaCO3,石灰乳是氢氧化钙,提供氢氧根离子和钙离子,更完全的沉淀镁离子和碳酸根离子,碳酸钠提供碳酸根离子用来沉淀过量的钙离子,;
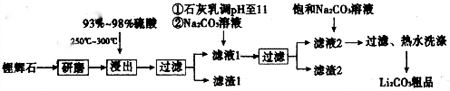
(3)依据图表分析可知碳酸锂溶解度随 温度升高减小;
(4)①Li2CO3溶于盐酸作电解槽的阳极液,阳极液中离子失电子,发生氧化反应,所以阳极反应为2C1--2e-=Cl2↑,阴极反应为2H++2e-=H2↑.离子选择透过膜只允许阳离子通过,电解过程中,Li+向阴极移动,而阴极电解后富余大量的OH-,阳极的Li+通过离子选择透过膜到阴极,这样阴极就得到比较纯净的LiOH.
②电解后向LiOH溶液中加入过量NH4HCO3溶液,氢氧化锂与碳酸氢铵反应生成碳酸锂.
解答 解:分析流程锂辉石主要成分为Li2O•Al2O3•4SiO2,含有少量Ca、Mg元素,研磨在加热条件下用浓硫酸酸浸后过滤得到Li2SO4,硫酸镁和硫酸钙,滤渣Ⅰ为Al2O3•4SiO2•H2O↓,滤液加入为石灰乳是氢氧化钙,提供氢氧根离子和钙离子,加入碳酸钠沉淀钙离子,更完全的沉淀镁离子和碳酸根离子,过滤得到滤液主要是Li2SO4,加入饱和碳酸钠沉淀锂离子为碳酸锂,滤渣2主要成分有Mg(OH)2和CaCO3,
(1)从滤渣1中分离出Al2O3的流程分析,加入酸溶解Al2O3•4SiO2•H2O,得到铝盐溶液和固体二氧化硅,过滤得到溶液硫酸铝,加入氨水或适量氢氧化钠溶液得到氢氧化铝沉淀,灼烧得到氧化铝;步骤Ⅱ中铝离子与氨水反应生成氢氧化铝沉淀,反应离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
故答案为:铝盐,氨水,Al(OH)3,Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
(2)石灰乳是氢氧化钙,提供氢氧根离子和钙离子,更完全的沉淀镁离子和碳酸根离子,增加Ca2+、OH-的浓度,有利于Mg(OH)2、CaCO3的析出,碳酸钠能沉淀过量的钙离子,反应的离子方程式为;Mg2++2OH-=Mg(OH)2↓,Ca2++CO32-=CaCO3↓
故答案为:Mg2++2OH-=Mg(OH)2↓,Ca2++CO32-=CaCO3↓;
(3)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”,图表中碳酸锂溶解度随温度升高减小,减少沉淀的损失,
故答案为:Li2CO3的溶解度随温度升高而减小,热水洗涤可减少Li2CO3的损失;
(4))①Li2CO3溶于盐酸作电解槽的阳极液,阳极液中氯离子失电子,发生氧化反应,所以阳极反应为2C1--2e-=Cl2↑,
故答案为:2C1--2e-=Cl2↑;
②电解后向LiOH溶液中加入过量NH4HCO3溶液,氢氧化锂与碳酸氢铵反应生成碳酸锂的方程式为:2LiOH+2NH4HCO3=Li2CO3+(NH4)2CO3+2H2O,
故答案为:2LiOH+2NH4HCO3=Li2CO3+(NH4)2CO3+2H2O.
点评 本题考查了物质生产流程的分析判断,流程分析,物质性质的应用是解题关键,主要是铝及其化合物性质的应用,氧化铝的提取方法,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | C7H6O2 | B. | C8H8O4 | C. | C14H12O2 | D. | C6H6O4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
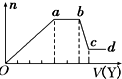 某无色稀溶液X中,可能含有如表所列离子中的某几种.
某无色稀溶液X中,可能含有如表所列离子中的某几种.| 阴离子 | CO32-、SiO32-、AlO2-、Cl- |
| 阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
| A. | 若Y是盐酸,则X中一定含有CO32-、SiO32-、AlO2-和Na+ | |
| B. | 若Y是NaOH溶液,则X中一定含有Al3+、Fe3+、NH4+、Cl- | |
| C. | 若Y是NaOH溶液,则ab段发生反应的离子方程式为:NH4++OH-═NH3↑+H2O | |
| D. | 若Y是NaOH溶液,则X中的Al3+、Mg2+、NH4+ 物质的量之比为1:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某物质焰色反应呈黄色,结论:该物质一定是钠盐 | |
| B. | 某溶液中滴加KSCN溶液,溶液不变红,再滴加氯水,变红,结论:原溶液一定有Fe2+ | |
| C. | 无色溶液中加入BaCl2溶液,有白色沉淀产生,再加稀硝酸,沉淀不消失,结论:原溶液一定含有SO42- | |
| D. | 无色溶液中加入稀盐酸,产生无色无味气体,该气体能使澄清石灰水变浑浊,结论:原溶液一定含有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$ Cu+H2O | |
| B. | NH4Cl+NaOH═NH3•H2O+NaCl | |
| C. | Cu+2H2SO4 (浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O | |
| D. | 2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡时SO2的转化率:A>B | |
| B. | 可逆反应从开始到平衡放出的热量:A<B | |
| C. | 平衡时混合气体的总物质的量:A<B | |
| D. | 平衡时的化学反应速率:A>B |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com