

科目:高中化学 来源:不详 题型:单选题
| A.二氯甲烷(CH2Cl2)分子的中心原子是SP3杂化,键角均为109°28′ |
| B.CH2O和ClO4-的中心原子上都含有孤对电子 |
| C.BCl3、PCl5、H2O分子中均有一个原子的最外层电子不满足了8e-稳定结构 |
| D.由原子间通过共价键形成的晶体一定比其他类别晶体熔、沸点高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.[Cu(NH3)4]2+和CH4两个粒子中中心原子Cu和C都是通过sp3杂化轨道成键 |
| B.气体单质中,一定有σ键,可能有π键 |
| C.两个原子之间形成共价键时,最多有一个σ键 |
| D.中心原子采用sp2,该分子一定是平面三角形 |
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题

查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题
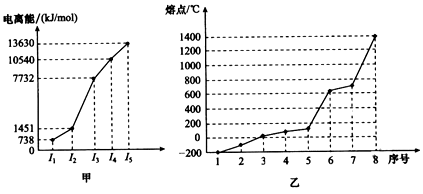
查看答案和解析>>
科目:高中化学 来源:同步题 题型:填空题

查看答案和解析>>
科目:高中化学 来源:专项题 题型:填空题

查看答案和解析>>
科目:高中化学 来源:期中题 题型:不定项选择题
查看答案和解析>>
科目:高中化学 来源:期末题 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com