
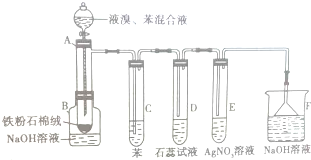
 如图为探讨苯和液溴反应改进的实验装置图,其中A为具支试管改制成的反应容器,在其下端开了一个小孔,并塞好石棉绒,实验时先加少量铁粉于石棉绒上,填写下列空白:
如图为探讨苯和液溴反应改进的实验装置图,其中A为具支试管改制成的反应容器,在其下端开了一个小孔,并塞好石棉绒,实验时先加少量铁粉于石棉绒上,填写下列空白:分析 (1)装置图中盛放液溴和苯混合液的仪器为分液漏斗,根据在催化剂的作用下,苯环上的氢原子被溴原子所取代,苯和液溴反应生成溴苯和溴化氢,溴与苯发生取代生成的溴苯为油状不溶于水的液体,密度大于水;
(2)根据苯和溴水不反应,发生萃取褪色现象,苯和液溴反应生成溴苯和溴化氢,溴化氢的溶液呈酸性;溴化氢能与硝酸银反应生成浅黄色的溴化银;
(3)B中的NaOH溶液作用是吸收反应生成的溴苯中溶解的溴单质,溴与氢氧化钠反应生成溴化钠、次溴酸钠和水;苯和液溴反应,铁作催化剂,C中苯的作用是除去挥发出的溴蒸气;
(4)根据防倒吸的原理解答,易溶于水的气体直接通入溶液会发生倒吸,中等吸收面积或与溶液隔离吸收,可以防止倒吸.
解答 解:(1)装置图中盛放液溴和苯混合液的仪器为分液漏斗,向反应容器A中逐滴加入液溴和苯的混合液,很快发生反应,此时可以看到的现象为,试管中出现白雾,氢氧化钠溶液底部有褐色油状物生成,在催化剂的作用下,苯环上的氢原子被溴原子所取代,生成溴苯,同时有易溶于水的溴化氢生成,反应的化学方程式为:C6H6+Br2 $\stackrel{FeBr_{3}}{→}$C6H5Br+HBr,
故答案为:分液漏斗;试管中出现白雾,氢氧化钠溶液底部有褐色油状物生成;C6H6+Br2 $\stackrel{FeBr_{3}}{→}$C6H5Br+HBr;
(2)苯和溴水不反应,将溴水和苯充分混合后的现象是,液体分层发生萃取褪色,上层颜色加深;苯和液溴反应生成溴苯和溴化氢,溴化氢的溶液呈酸性,能证明苯和液溴发生的是取代反应,而不是加成反应的证据是反应开始后D中可看到的现象为,D中紫色的石蕊试剂显红色,溴化氢与硝酸银反应生成浅黄色的溴化银和硝酸,且溴化银不溶于硝酸,E中有浅黄色的沉淀;
故答案为:液体分层发生萃取褪色,上层颜色加深;D试管中显红色;试管中有浅黄色的沉淀;
(3)B中的NaOH溶液作用是吸收反应生成的溴苯中溶解的溴单质,溴与氢氧化钠反应生成溴化钠、次溴酸钠和水,反应的离子方程式为:2OH-+Br2=Br-+BrO-+H2O;苯和液溴反应,铁作催化剂,苯环上的氢原子被溴原子所取代,生成溴苯,同时生成溴化氢,该反应为放热反应,溴易挥发,所以,试管C中苯的作用是除去挥发出的溴蒸气,
故答案为:除去溶于溴苯中的溴;2OH-+Br2=Br-+BrO-+H2O;催化剂;除去挥发出的溴蒸气;
(4)装置F中倒置的漏斗有缓冲作用,气体能充分被吸收且防止倒吸,故答案为:气体能充分被吸收且防止倒吸.
点评 本题考查了苯的取代反应实验,考查的知识点有反应方程式的书写、产物的判断、蒸汽的成分及性质,综合性较强,难度中等,注意苯能和液溴发生取代反应,和溴水不反应.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应达到平衡时,放出的热量等于92.4KJ | |
| B. | 达到平衡后向容器中通入1mol氦气,平衡不移动 | |
| C. | 降低温度和缩小容器体积均可使该反应的平衡常数增大 | |
| D. | 若达到平衡时N2的转化率为20%,则平衡时容器内的压强是起始时的80% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属元素A的单质不能把金属元素B从它的盐溶液中置换出来,一定可以说明金属性:A<B | |
| B. | 根据反应2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,可说明C的非金属性比Si强 | |
| C. | 周期表中第n周期第n主族的元素均为金属 | |
| D. | 按照元素周期表的排布规律,非金属元素最多为23种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
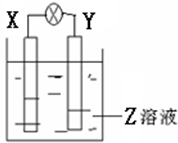 如图所示装置中,观察到电流计指针偏转,X棒变重,Y棒变轻,由此判断下表中所列X、Y、Z物质,其中可以成立的是( )
如图所示装置中,观察到电流计指针偏转,X棒变重,Y棒变轻,由此判断下表中所列X、Y、Z物质,其中可以成立的是( )| X | Y | Z | |
| A | 锌 | 铜 | 稀硫酸溶液 |
| B | 铜 | 铁 | 稀盐酸 |
| C | 锌 | 铜 | 硝酸银溶液 |
| D | 碳 | 锌 | 硝酸铜溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与$\underset{\stackrel{16}{\;}}{8}{O}_{2}$互为同位素 | B. | 与氧气具有相同的化学性质 | ||
| C. | 与氧气互为同素异形体 | D. | 与同质量的氧气具有相同的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com