
下列实验操作中正确的是
A.定容
B.吸收HCl气体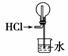
C.酸碱中和滴定
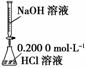
D.用CCl4萃取溴水中的溴
科目:高中化学 来源: 题型:
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y 同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列有关说法
 正确的是( )
正确的是( )
A.洗气瓶中产生的沉淀是碳酸钡
B.在Z导管出来的气体中无二氧化碳
C.洗气瓶中产生的沉淀是硫酸钡
D.在Z导管口有红棕色气体出现
查看答案和解析>>
科目:高中化学 来源: 题型:
向盛有KI溶液的试管中加入少许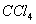 后滴加氯水,
后滴加氯水,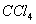 层变成紫色。如果继续向试管中滴加氯水,振荡,
层变成紫色。如果继续向试管中滴加氯水,振荡,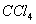 层会逐渐变浅,最后变成无色。 完成下列填空:
层会逐渐变浅,最后变成无色。 完成下列填空:
1) 写出并配平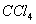 层由紫色变成无色的化学反应方程式
层由紫色变成无色的化学反应方程式
2)整个过程中的还原剂是___。
3)把KI换成KBr,则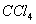 层变为_____色:继续滴加氯水,
层变为_____色:继续滴加氯水,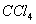 层的颜色没有变化。
层的颜色没有变化。 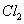 、
、 、
、 氧化性由强到弱的顺序是______。
氧化性由强到弱的顺序是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
取少量Fe2O3粉末(红棕色)加入适量盐酸,发生反应的化学方程式:______________________________,反应后得到的溶液呈________色。用此溶液分别做如下实验:
(1)取少量溶液置于试管中,滴入几滴NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为_______________________________,
此反应属于______________________________。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈________色,即制得Fe(OH)3胶体。
(3)取另一只小烧杯也加入20 mL蒸馏水,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到________烧杯中的液体产生丁达尔效应。这个实验可以用来区别__________________________________。
(4)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量的稀HI溶液,边滴加边振荡,会出现一系列变化。
①先出现红褐色沉淀,原因是__________________________________。
②随后沉淀溶解,溶液呈黄色,写出此反应的离子方程式:_________。
② 最后溶液颜色加深,原因是____________________。(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
读下列药品标签,有关分析不正确的是
| 选项 | A | B | C | D |
| 物品标签 |
| 药品:×××
|
|
|
| 分析 | 该试剂应装在橡胶塞的细口瓶中 | 该药品不能与 皮肤直接接触 | 该物质受 热易分解 | 该物质浓度为 18.4 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
分离或提纯下列各组混合物所选用的方法最合理的是
A.除去C2H6中的C2H4——高温、高压、催化剂作用下通入氢气
B.除去O2中的N2——通过灼热的Cu网
C.除去CO2中的SO2——通入饱和Na2CO3溶液,洗气
D.分离NaNO3和BaSO4的混合物——溶解、过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
已知废旧干电池中的填充物主要有二氧化锰、炭黑、氯化锌、氯化铵、淀粉糊、Mn2O3、ZnO、FeO、汞的化合物等。某实验小组的同学拟回收废旧电池中的成分,主要操作流程如下图:
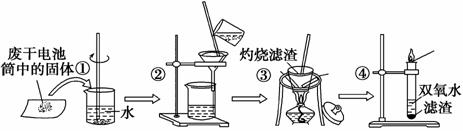
试回答下列问题。
(1)步骤①用玻璃棒搅拌的目的是_______________________________________
___________________________________________________________________;
步骤②过滤后,滤液中的主要溶质有____________(填化学式);步骤③中灼烧的目的是__________________________________ ______________________________________。
______________________________________。
(2)经过步骤③得到的是粗制二氧化锰,要得到精制的二氧化锰还需将粗制二氧化锰用稀硝酸洗涤和蒸馏水洗涤,稀硝酸的作用是___________________________________
______ ______________________________________________________________。
______________________________________________________________。
(3)写出步骤④中发生反应的化学方程式:__________________________________
________________________________________________________________________,
经过步骤②得到的固体干燥后,用氯酸钾与之混合加热的实验________(填“能”或“不能”)代替实验④。
(4)已知NH4Cl和ZnCl2的溶解度(g/100 g水)如下表:
| 温度(℃) | 20 | 30 | 40 | 60 | 80 |
| NH4Cl | 37.2 | 31.4 | 45.8 | 65.6 | 77.3 |
| ZnCl2 | 396 | 437 | 452 | 541 | 614 |
从滤液中分离NH4Cl和ZnCl2的方法是___________________________________。
(5)从有害物质必须特殊处理的角度考虑,上述设计不合理的地方是___________________________________ _____________________________________。
_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定质量的Mg、Zn、Al混合物与足量稀H2SO4反应,生成H20.125mol,原混合物的质量可能是 ( )
A.2g B.4g C.8g D.10g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com