
 可由有机化工原料R和其他有机试剂通过加成、水解、氧化、缩聚反应得到,则R是( )
可由有机化工原料R和其他有机试剂通过加成、水解、氧化、缩聚反应得到,则R是( )| A、1-丁烯 | B、2-丁烯 |
| C、1,3-丁二烯 | D、乙烯 |
 可知,合成该高分子化合物,为缩聚反应,需要HOOCCOOH、OHCH2CH2OH两种原料,乙二醇连续氧化生成乙二酸,乙二醇可由烯烃加成、水解制备,以此来解答.
可知,合成该高分子化合物,为缩聚反应,需要HOOCCOOH、OHCH2CH2OH两种原料,乙二醇连续氧化生成乙二酸,乙二醇可由烯烃加成、水解制备,以此来解答. ,为缩聚反应,需要HOOCCOOH、OHCH2CH2OH两种原料发生酯化反应制取,
,为缩聚反应,需要HOOCCOOH、OHCH2CH2OH两种原料发生酯化反应制取,

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
| A、恒温下向溶液中加CaO,溶液的pH不变 |
| B、给溶液加热,溶液的pH升高 |
| C、向溶液中加入Na2CO3溶液,其中固体质量不变 |
| D、向溶液中加入少量NaOH固体,Ca(OH)2固体质量增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:
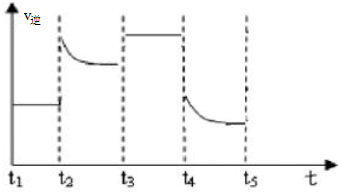
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大理石溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O |
| B、FeBr2溶液中通入少量的Cl2:Cl2+2Fe2+=2Fe3++2Cl- |
| C、向澄清石灰水中通入少量CO2:OH-+CO2=HCO3- |
| D、酸性氢氧燃料电池的正极反应:H2-2e-=2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
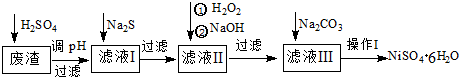
查看答案和解析>>
科目:高中化学 来源: 题型:
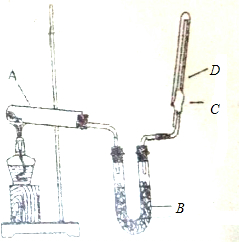 如图所示,实验室用NH4Cl和Ca(OH)2制取NH3.
如图所示,实验室用NH4Cl和Ca(OH)2制取NH3. 查看答案和解析>>
科目:高中化学 来源: 题型:
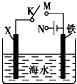
| A、X为锌,开关K置于M处 |
| B、X为锌,开关K置于N处 |
| C、X为铜,开关K置于M处 |
| D、X为碳棒,开关K置于N处 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com