
����Ŀ��ij��ѧ��ȤС��Ҫ����к��ȵIJⶨ��
(1)ʵ�����ϱ��д�С�����ձ�����ĭ���ϡ���ĭ���ϰ塢��ͷ�ιܡ����β����������0.5 molL-1���ᡢ0.55 molL-1NaOH��Һ��ʵ����ȱ�ٵIJ�����Ʒ��__��__��
(2)ʵ�����ܷ��û���ͭ˿��������滷�β����������__������������������������ԭ����__��
(3)���Ǽ�¼��ʵ���������£�
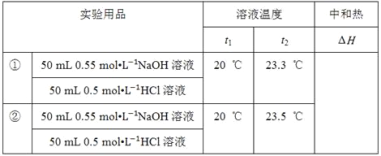
��֪��Q=cm(t2��t1)����Ӧ����Һ�ı�����cΪ4.18 J����1g��1�������ʵ��ܶȾ�Ϊ1 gcm��3��
�� ��������ϱ���H=__������2λС������
�ڸ���ʵ����д��NaOH��Һ��HCl��Һ��Ӧ���Ȼ�ѧ����ʽ��__��
(4)����KOH����NaOH���Բⶨ���__��������������������Ӱ�죻���ô������HCl��ʵ�飬�Բⶨ���__��������������������Ӱ�졣
���𰸡���1����Ͳ���¶ȼƣ�
��2�����ܣ��������ȣ�����ɢʧ��������3���٩�56.85��
��HCl��aq��+NaOH��aq��=NaCl��aq��+H2O��l����H=��56.8kJmol��1��
��4���ޣ��У�
��������
��1���к��ȵIJⶨ�����У���Ҫ����Ͳ��ȡ����Һ������Һ���������Ҫʹ���¶ȼƲ����¶ȣ����Ի�ȱ���¶ȼƺ���Ͳ��
��2�������û���ͭ˿��������滷�β������������Ϊͭ˿��������ȵ������壬������ʧ��
��3������1��ʵ�鷴Ӧǰ���¶Ȳ�Ϊ��3.3������2��ʵ�鷴Ӧǰ���¶Ȳ�Ϊ��3.5����ƽ���¶Ȳ�Ϊ3.4����50 mL0.55 molL��1NaOH��Һ��50 mL0.5 molL��1HCl��Һ��������Ϊm=100mL��1g/cm3=100g��c=4.18J/��g���������빫ʽQ=cm��T������0.05mol��ˮ�ų�����Q=4.18J/��g������100g��3.4��=1421.2J=1.4212kJ��������0.025mol��ˮ�ų�����Ϊ��1.4212kJ����������1mol��ˮ�ų�����Ϊ��![]() =56.85kJ������ʵ���õ��к�����H=��56.85kJ/mol��
=56.85kJ������ʵ���õ��к�����H=��56.85kJ/mol��
��ϡ�����NaOHϡ��Һ��Ӧ����1molˮ����56.8KJ���÷�Ӧ���Ȼ�ѧ����ʽΪ��HCl��aq��+NaOH��aq��=NaCl��aq��+H2O��l����H=��56.8kJmol��1��
��4��KOH����NaOH����ǿ������к��ȵĸ��������KOH����NaOH���Բⶨ�����Ӱ�죻����Ϊ���ᣬ�������Ϊ���ȹ��̣������ô������HCl��ʵ�飬��Ӧ�ų�������С��56.8kJ������Hƫ��


 ������Ӧ���ϵ�д�
������Ӧ���ϵ�д� ��ʦ�㾦�ִʾ��ƪϵ�д�
��ʦ�㾦�ִʾ��ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������£����淴Ӧ��2NO��g��+O2��g��![]() 2NO2��g��������̶����ܱ������н��У��ﵽƽ��״̬�ı�־���ǣ�������
2NO2��g��������̶����ܱ������н��У��ﵽƽ��״̬�ı�־���ǣ�������
����λʱ��������n mol O2��ͬʱ����2n mol NO2����λʱ��������n mol O2��ͬʱ����2n mol NO����NO2��NO��O2��ʾ�ķ�Ӧ���ʵı�Ϊ2��2��1��״̬������������ɫ���ٸı��״̬�����������ܶȲ��ٸı��״̬����������ѹǿ���ٸı��״̬����������ƽ����Է����������ٸı��״̬��
A. �٢ܢޢ� B. �ڢۢݢ� C. �٢ۢܢ� D. ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ���³�ѹ�£�������Ħ����������71 g
B. 1 mol H2SO4�к���2 mol��Ԫ��
C. ij���ʵ�Ħ���������Ǹ����ʵ���Է������������ԭ������
D. 2 g����������ԭ����ĿԼΪ0.5��6.02��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��µĶ��������У���������Щ���������ٷ����仯ʱ��������ӦA(g)��2B(g)![]() C(g)��D(g)�Ѵﵽƽ��״̬
C(g)��D(g)�Ѵﵽƽ��״̬
�ٻ�������ѹǿ�� �ڻ��������ܶȡ� �� B�����ʵ���Ũ�ȡ� �� �������������ʵ��� �ݻ�������ƽ����Է��������� ��v(C)��v(D)�ı�ֵ�� ������������������������������ ����C��D�ķ�����֮��Ϊ1��1
A. �٢ڢۢܢݢޢߢ� B. �٢ۢܢ� C. �٢ڢۢܢݢ� D. �٢ۢܢݢ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������
��1������֮��Ϊ16��7��6����������SO2��CO��NO��������֮��Ϊ___����ԭ����֮��Ϊ____����ͬ�����µ����֮��Ϊ____��
��2����״���£�1.7gNH3���״����___LH2S������ͬ��Ŀ����ԭ�ӡ�
��3��ij����������Ļ�ѧʽΪRO2����״���£�1.28g������������Ϊ448mL������������Ħ������Ϊ____��R�����ԭ������Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��20��ʱ��NaCl�ܽ���ˮ��ʵ���������±���ʾ
ʵ����� | ˮ������/g | �����NaCl����/g | δ�ܵ�NaCl����/g |
10 | 2 | 0 | |
10 | 3 | 0 | |
10 | 4 | 0.4 |
����������ȷ����( )
A. ʵ������õ���ҺΪ������Һ B. ʵ������õ���ҺΪ������Һ
C. 20��ʱNaCl���ܽ��Ϊ30g D. ʵ���������Һ��������������Ϊ16.7%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��EPR��(![]() )�㷺Ӧ�������������������÷�ˮ���ϡ����ߵ��»��ס����Ƚ��ܡ������ܷ�����������Ӽ���������Ʒ��
)�㷺Ӧ�������������������÷�ˮ���ϡ����ߵ��»��ס����Ƚ��ܡ������ܷ�����������Ӽ���������Ʒ��
PC����( ![]() )���������ã����������������ɻ��ĵ��粣���Լ��۾��ȡ����ǵĺϳ�·�����£�
)���������ã����������������ɻ��ĵ��粣���Լ��۾��ȡ����ǵĺϳ�·�����£�

��֪����RCOOR1 + R2OH ![]() RCOOR2 + R1OH
RCOOR2 + R1OH
��B��F��G��H��J�������У��˴Ź�������ֻ��һ�����շ塣
(1)B�Ľṹ��ʽ��_______________��
(2)A��D�ķ�Ӧ���ͣ�_______________��
(3)D��E�ķ�Ӧ������_______________��
(4)E�й��������ƣ�_______________��
(5)E��F�Ļ�ѧ����ʽ��_______________��
(6)H�Ľṹ��ʽ��_______________��
(7)��ӦII�Ļ�ѧ����ʽ��_______________��
(8)����˵����ȷ���ǣ�_______________��
a����ӦI��ԭ��������Ϊ100%
b��1mol J��������NaOH��Һ��Ӧ������2molNaOH
c��CH3OH�ںϳ�PC���Ϲ����п���ѭ������
(9)��ӦI�����У����Եõ�����ͬ�����������M��Ϊͬ���칹�壬��д������һ�ֽṹ��_______________��
(10)A ![]() N
N ![]() ����+F�����ƶ�N�Ľṹ��_______________
����+F�����ƶ�N�Ľṹ��_______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪25��ʱCH3COOH�ĵ��볣��K=1.6��10-5�����¶�����20ml 0.01molL-1 CH3COOH��Һ����μ���0.01molL-1 KOH��Һ����pH�仯������ͼ��ʾ�������¶ȱ仯���������й�������ȷ����

A. a����Һ��c��H+��Ϊ4.0��10-5mol/L
B. c����Һ�е�����Ũ�ȴ�С˳��Ϊc��K+��>c��CH3COO-��>c��H+��=c��OH-��
C. V=20
D. a��b��c������ˮ�ĵ���̶�������c��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��100��ʱ����0.1 mol N2O4����1 L�ܱյ���ƿ�У�Ȼ����ƿ����100���ĺ��²��У���ƿ�ڵ�������Ϊ����ɫ��N2O4(g) ![]() 2NO2 (g)�����н��۲���˵��������Ӧ�ڸ��������Ѿ��ﵽ��Ӧ�ȵ����� ��
2NO2 (g)�����н��۲���˵��������Ӧ�ڸ��������Ѿ��ﵽ��Ӧ�ȵ����� ��
��N2O4������������NO2����������֮��Ϊ1��2����NO2������������NO2����������ȣ�����ƿ�������ѹǿ���ٱ仯������ƿ��������������ٱ仯����NO2�����ʵ���Ũ�Ȳ��ٸı䣻����ƿ���������ɫ���ټ������ƿ�������ƽ����Է����������ٱ仯������ƿ��������ܶȲ��ٱ仯��
A. �ڢۢޢ� B. �٢ܢ�
C. ֻ�Т٢� D. ֻ�Тߢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com