
ijѧ����0.20mol��L-1�ı�NaOH��Һ�ζ�δ֪Ũ�ȵ����ᣬ��������£�
�� ������ˮϴ�Ӽ�ʽ�ζ��ܣ�������ע��NaOH��Һ����0���̶������ϣ�
�� �̶��õζ��ܲ�ʹ�ζ��ܼ������Һ�壻
�� ����Һ������0����0���̶������£������¶�����
�� ��ȡ20.00mL����Һע��ྻ����ƿ�У�������3�η�̪��Һ��
�� �ñ�Һ�ζ����յ㣬���µζ���Һ�������
��ش�
��1�����ϲ����д�����ǣ����ţ� ���ô�������ᵼ�²ⶨ������ƫ����ƫС������Ӱ�족�� ��
��2������ȡ20.00mL����Һע����ˮ����ƿ�У��ᵼ�½�����ƫ����ƫС������Ӱ�족�� ��
��3���жϵζ��յ�������ǣ� ��

��4����ͼ��ij�εζ�ʱ�ĵζ����е�Һ�棬�����Ϊ mL��
��5�������������ݣ�
�ζ����� | ���������mL�� | ���ռ������mL�� | |
�ζ�ǰ���� | �ζ������ | ||
��һ�� | 20.00 | 0.40 | 20.40 |
�ڶ��� | 20.00 | 0.00 | 22.60 |
������ | 20.00 | 4.00 | 24.00 |
��������������Һ��Ũ�ȣ� mol/L��
 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д� �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �� | B�� | �٢� | C�� | �٢ڢ� | D�� | �٢ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ӱ�ʡ��һ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���й��ڻ�ѧ��Ӧ���͵������У���ȷ����
A�����������κ�ˮ�ķ�Ӧ�����кͷ�Ӧ
B�����ֽⷴӦһ��û�е��ʲμ�
C������һ�ֵ��ʺ�һ�ֻ�����ķ�Ӧһ�����û���Ӧ
D���ֽⷴӦ��������һ���е���]
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�߶��ϵ�һ��ѧ�ο��Ի�ѧ���������棩 ���ͣ�ѡ����
�����£�1mol��ѧ���ֽ����̬ԭ������Ҫ��������E��ʾ�����ݱ�����Ϣ�ж�����˵������ȷ���ǣ� ��
���ۼ� | H��H | F��F | H��F | H��Cl | H��I |
E/(kJ��mol��1) | 436 | 157 | 568 | 432 | 298 |
A��432kJ��mol��1>E(H��Br)>298kJ��mol��1
B���������ȶ��Ĺ��ۼ���H��F��
C��H2(g)��2H(g)��H=+436kJ��mol��1
D��H2(g)+F2(g)=2HF(g)��H=��25kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�߶��ϵ�һ��ѧ�ο��Ի�ѧ���������棩 ���ͣ�ѡ����
����ɫ��ѧ������Ҫ����֮һ�ǴӼ�������������ƿ��еĻ�ѧ��Ӧ��ʹԭ�ӳ�����ã���������Ⱦ����л�ѧ��Ӧ�����ϡ���ɫ��ѧ��������ǣ� ��
A���������飺CH2=CH2+HCl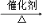 CH3CH2Cl
CH3CH2Cl
B���Ƽ���ϩ�������CH3C��CH+CO+CH3OH  CH2=C��CH3��COOCH3
CH2=C��CH3��COOCH3
C����CuSO4��2Cu+O2 = 2CuO��CuO+H2SO4��ϡ���TCuSO4+H2O
D����Cu��NO3��2��Cu+4HNO3��Ũ���TCu��NO3��2+2NO2��+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�߶���10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
Ҫ��ȥMgCl2������Һ��������FeCl3������ѡ�õ��Լ��� �� ��
A��MgO B��MgCO3 C��NaOH D��Mg(OH)2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| MnO2 | �����Թ���� | �۲��� | ��Ӧ��������ʱ�� |
| ��ĩ״ | ���� | ���ҷ�Ӧ�������ǵ�ľ����ȼ | 3.5min |
| ��״ | �� | ��Ӧ���������Ǻ�����ľ��δ��ȼ | 30min |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com