
【题目】下列事实,不能用勒夏特列原理解释的是
A.向氯水中加入AgNO3溶液后,溶液颜色变浅
B.对2HI(g) ![]() H2(g)+I2(g)平衡体系,体积缩小,压强增大可使颜色变深
H2(g)+I2(g)平衡体系,体积缩小,压强增大可使颜色变深
C.合成氨反应中用过量氮气与氢气反应可以提高氢气的转化率
D.将混合气中的氨气液化后不停的分离出来,有利于合成氨的反应
 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:
【题目】氰化钠(化学式NaCN,C元素+2价,N元素-3价)是白色结晶颗粒、易潮解、剧毒、易溶于水、水溶液呈碱性。氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻污染。
(1)氰化钠溶液呈碱性,其原因是 (用离子方程式解释)。
(2)用双氧水处理NaCN产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,写出该反应的化学方程式:________。
某化学兴趣小组在实验室制备硫代硫酸钠,并检测含氰化钠废水用硫代硫酸钠溶液处理后能否达标排放。
【实验一】实验室通过如下图所示装置制备Na2S2O3。

(3)装置a中盛装Na2 S03固体的仪器名称是 ,装置b的作用是________。
(4)装置c中的产物有Na2S2O3和CO2气体等,实验结束后,装置d中的溶质有NaOH、Na2CO3,还可能有 (填化学式)。
(5)实验结束后,在e处最好连接盛____(填“NaOH溶液”“水”或“CCl4”)的注射器,再关闭K2打开K1,防止拆除装置时污染空气。
【实验二】测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。已知:
①废水中氰化钠的最高排放标准为0.50 mg.L-l。
![]() ,AgI呈黄色,且CN-优先与Ag+反应,
,AgI呈黄色,且CN-优先与Ag+反应,
实验如下:取25.00 mL处理后的氰化钠废水于锥形瓶中并滴加几滴KI溶液作指示剂,用1.000×1 0-4mol.L-l的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为2.50 mL。
(6)滴定终点的判断方法是________。
(7)处理后的废水中氰化钠的含量为 mg.L-l。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列物质的用途的说法错误的是
A.酚类化合物有毒,不能用于杀菌消毒
B.乙二醇可用于配制汽车防冻液
C.部分卤代烃可用作灭火剂
D.甲醛的水溶液(福尔马林)可用于防腐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组研究可逆反应AsO43—+2I—+2H+![]() AsO33—+I2+H2O时,设计了如图所示的原电池:
AsO33—+I2+H2O时,设计了如图所示的原电池:

(1)电池工作时,盐桥中的阴离子向 极移动(填C1或C2);若向B池里滴加NaOH溶液,平衡向 方向移动,此时C2极的电极反应式为 。
(2)下列判断正确的是 。
a.微安表指针为0时,该反应处于平衡状态。
b.向A池中加入淀粉溶液,溶液变蓝说明该反应处于平衡状态。
c.AsO43—、AsO33—离子浓度相等时,该反应处于平衡状态。
(3)若在5min时间内电路中通过了1.204×104库伦电量,用I—浓度的变化来表示的化学反应速率为 。
(4)该反应的平衡常数表达式K= 。若升高温度,K值增大,则正反应的△H 0。(填“>”、“<”或“=”)
(5)已知反应达到平衡时,AsO43—离子转化率为25%,则I—离子的转化率 。
a.大于25% b.小于25%
c.等于25% d无法确定
(6)反应达到平衡后,若将AsO43—、I—、H+、AsO33—、I2的浓度均减少到原来的一半,上述平衡向 方向移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气在氯气中燃烧时发出苍白色火焰,在反应过程中,破坏1mol氢气中的化学键消耗的能量为a kJ,破坏1mol氯气中的化学键消耗的能量为b kJ,形成1mol HCl中的化学键释放的能量为c kJ,下列关系中正确的是( )
A.b>c
B.a+b>2c
C.a+b<c
D.a+b<2c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,下列叙述不是可逆反应A(g)+2B(g)![]() 2C(g)达到平衡状态标志的是
2C(g)达到平衡状态标志的是
①C的生成速率与C的分解速率相等;
②单位时间生成amol A,同时生成3amolB;
③A、B、C的浓度不再变化;
④混合气体平均摩尔质量不再变化
⑤混合气体的总压强不再变化;
⑥混合气体的物质的量不再变化;
⑦单位时间内消耗amol A,同时生成3amol B ⑧A、B、C的分子数比为1:3:2
A. ②⑧ B. ①⑥ C. ②④ D. ③⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以Pt为电极,电解含有0.10molM+和0.10molN3+(M+、N3+均为金属阳离子)的溶液,阴极析出金属单质或气体的总物质的量(y)与导线中通过电子的物质的量(x)的关系如右图。对离子氧化能力的强弱判断正确的是(选项中H+为氢离子)

A. M+>H+>N3+
B. M+>N3+>H+
C. N3+>H+>M+
D. 条件不足,无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2。某同学在实验中对NH3与NO2反应进行了探究。回答下列问题:
(1)氨气的制备
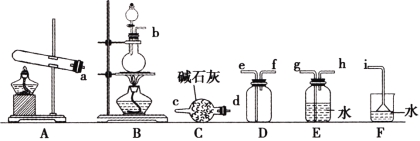
①氨气的发生装置可以选择上图中的 ,反应的化学方程式为 。
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→ (按气流方向,用小写字母表示)
(2)氨气与二氧化氮的反应
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2 (两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。
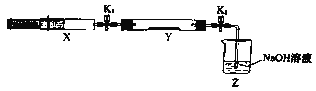
操作步骤 | 实验现象 | 解释原因 |
打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中 | ①Y管中 | ②反应的化学方程式 |
将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝聚 |
打开 | ③ | ④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com