
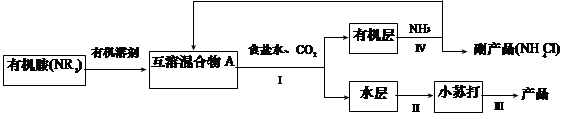
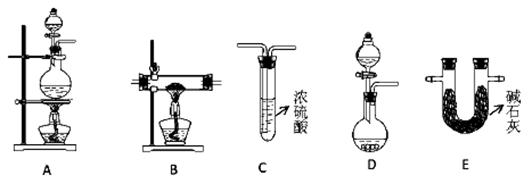
 N2+ 3Cu + 3H2O(2分);DEBC(2分);干燥N2(1分)并除去其中的NH3(1分)
N2+ 3Cu + 3H2O(2分);DEBC(2分);干燥N2(1分)并除去其中的NH3(1分) N2+ 3Cu + 3H2O;需要的NH3 以生石灰和浓氨水作原料,因此需要用D用来制取氨气,氨气是碱性气体,不能用浓硫酸干燥,应该用E装置(碱石灰)干燥氨气。在B中反应后,剩余的氨气可用C装置来除去,同时C装置中的浓硫酸还能干燥氮气。所以按气流从左到右,整套装置的连接顺序是DEBC。
N2+ 3Cu + 3H2O;需要的NH3 以生石灰和浓氨水作原料,因此需要用D用来制取氨气,氨气是碱性气体,不能用浓硫酸干燥,应该用E装置(碱石灰)干燥氨气。在B中反应后,剩余的氨气可用C装置来除去,同时C装置中的浓硫酸还能干燥氮气。所以按气流从左到右,整套装置的连接顺序是DEBC。

 全能测控期末小状元系列答案
全能测控期末小状元系列答案 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


 。
。 CoO2+LiC6,写出该电池放电时的正极反应式 。
CoO2+LiC6,写出该电池放电时的正极反应式 。
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.工业上金属Mg、Al都是用电解其相应的氯化物水溶液制得的 |
| B.日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 |
| C.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
| D.为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
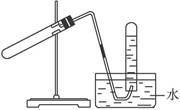
| A.加热NaHCO3制CO2 | B.用Cu与稀HNO3反应制NO |
| C.用NH4Cl与浓NaOH溶液反应制NH3 | D.用KMnO4与浓HCl反应制Cl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.称取的Na2CO3固体中有杂质 |
| B.溶解Na2CO3固体时,因搅拌剧烈使烧杯中的溶液溅出少量 |
| C.没有洗涤烧杯及玻璃棒 |
| D.定容时发现液面高于刻度线,用胶头滴管吸出多余的溶剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com