
A、 |
B、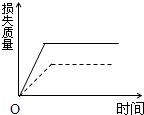 |
C、 |
D、 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图为周期表中的一部分.已知A、B、C、D均为短周期元素,A与D原子序数之和为C原子序数的1.5倍.
如图为周期表中的一部分.已知A、B、C、D均为短周期元素,A与D原子序数之和为C原子序数的1.5倍.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液的导电能力比盐酸弱 |
| B、1mol/L醋酸溶液中c(H+)=0.01 mol?L-1 |
| C、醋酸能与水任何比例互溶 |
| D、与等物质的量的NaOH恰好完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某研究性学习小组设计实验方案来研究稀硝酸与铜反应生成NO.
某研究性学习小组设计实验方案来研究稀硝酸与铜反应生成NO.查看答案和解析>>
科目:高中化学 来源: 题型:
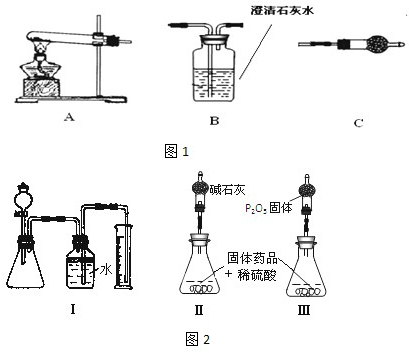
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 实验操作 | 现象与结论 | 离子方程式 |
| 第1步 | 取2~3mL溶液装于试管,向试管中滴加几滴KSCN溶液 | ||
| 第2步 | 若溶液紫色褪去,则溶液 含有Fe2+;若无明显变化, 则不含Fe2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com