
【题目】某同学用托盘天平称量镁粉25.3g(1g以下用游码),他把镁粉放在右盘,当天平平衡时,所称取的镁粉的实际质量是( )
A.25.2gB.24.8gC.24.7gD.25.7g
科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.请回答下列问题:
X | Y | |
Z | W |
(1)元素Z位于周期表中第_____周期,_____族;
(2)比较X与Y的气态氢化物的稳定性:_____(写化学式);
(3)XW2的电子式为_____;
(4)比较X、Y、Z、W四种原子半径由大到小关系:_____;
(5)X和W形成的化合物属于_____ (填“离子化合物”、或“共价化合物”),该化合物中存在的微粒间作用力有:_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒氧化还原电池是一种新型可充电池,不同价态的含钒离子作为正极和负极的活性物质,分别储存在各自的酸性电解液储罐中。其结构原理如图所示,该电池放电时,右槽中的电极反应为:V2+-e-=V3+,下列说法正确的是

A. 放电时,右槽发生还原反应
B. 放电时,左槽的电极反应式:VO2++2H++e-=VO2++H2O
C. 充电时,每转移1mol电子,n(H+)的变化量为1mol
D. 充电时,阴极电解液pH升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某烃A的分子组成和结构,对这种烃进行以下实验:
![]() 取一定量的该烃,使其充分燃烧后的气体通过干燥管,干燥管增重
取一定量的该烃,使其充分燃烧后的气体通过干燥管,干燥管增重![]() ;再通过石灰水,石灰水增重
;再通过石灰水,石灰水增重![]() 。
。
![]() 经测定,该烃(气体)
经测定,该烃(气体)![]() 在标准状况下的密度为
在标准状况下的密度为![]() 。
。
现以A为主要原料合成乙酸乙酯,其合成路线如图1所示。
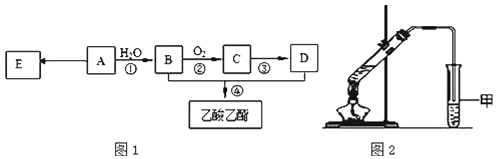
(1)![]() 该烃A能与______g溴发生加成反应;加成产物需______mol溴蒸气完全取代;
该烃A能与______g溴发生加成反应;加成产物需______mol溴蒸气完全取代;
(2)B中官能团的名称是_________,B通过两次氧化可得到D,也可通过加入的氧化试剂为______![]() 任填一种
任填一种![]() 直接氧化为D.
直接氧化为D.
(3)E是常见的高分子材料,写出E的结构简式__________;合成E的反应类型_______________;
(4)某同学用如图2所示的实验装置制取少量乙酸乙酯。实验结束后,试管甲中上层为透明的、不溶于水的油状液体。
①实验开始时,试管甲中的导管不伸入液面下的原因是__________________;
②上述实验中饱和碳酸钠溶液的作用是__________________![]() 填字母
填字母![]() ;
;
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.降低乙酸乙酯在水中的溶解度,有利于分层析出
D.加速酯的生成,提高其产率
![]() 在实验室利用B和D制备乙酸乙酯的实验中,若用1molB和1molD充分反应,不能生成1mol乙酸乙酯,原因是______________________________.
在实验室利用B和D制备乙酸乙酯的实验中,若用1molB和1molD充分反应,不能生成1mol乙酸乙酯,原因是______________________________.
(5)与乙酸乙酯互为同分异构体且能与![]() 反应生成CO2的有机物的结构简式为:
反应生成CO2的有机物的结构简式为:
________________、_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验事故的处理方法正确的是( )
A.不慎将酸或碱液溅入眼内,立即闭上眼睛,用手揉擦
B.实验桌上的酒精灯倾倒了燃烧起来,应立即用湿布扑灭
C.皮肤上溅有较多的浓硫酸,应立即用水冲洗
D.配制硫酸溶液时,可先在量筒中加入一定体积水,再在搅拌条件下慢慢加入浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将1.000mol·L-1盐酸滴入20.00mL 1.000mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法正确的是( )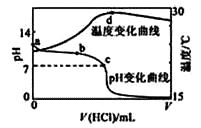
A.a点由水电离出的c(H+)=1.0×10-14mol/L
B.b点:c(NH4+)+c(NH3·H2O) > c(Cl-)
C.c点:反应消耗的HCl 和NH3·H2O 的关系为:n(HCl)= n(NH3·H2O)
D.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在金刚石的晶体中,含有由共价键形成的碳原子环,其中最小的环上所需碳原子数及每个碳原子上任意两个C--C键间的夹角是( )
A.6个120° B.5个108° C.4个109°28′ D.6个109°28′
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表是常温下几种弱电解质的电离平衡常数:
酸或碱 | 电离常数(Ka或Kb) | 难(微)溶物 | 溶度积常数(Ksp) |
CH3COOH | 1.8×10-5 | BaSO4 | 1×10-10 |
HNO2 | 4.6×10-4 | BaCO3 | 2.6×10-9 |
HCN | 5×10-10 | CaSO4 | 7×10-5 |
HClO | 3×10-8 | CaCO3 | 5×10-9 |
NH3·H2O | 1.8×10-5 |
请回答下面问题:
(1)上述四种酸中,酸性最弱的是 (用化学式表示)。下列能使醋酸溶液中CH3COOH的电离程度增大,而电离常数不变的操作是(填序号)。
A.升高温度 B.加水稀释
C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈 (选填“酸性”“中性”或“碱性”),理由是 , 溶液中各离子浓度大小的关系是。
(3)物质的量1∶1的NaCN和HCN的混合溶液,其pH>7,该溶液中离子的浓度从大到小排列为。
(4)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如:BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量的BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度达到0.01mol·L-1以上,则溶液中CO32-物质的量浓度应 ≥mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,向20mL0.1mol·L-1MOH溶液中滴加0.1mol·L-1CH3COOH溶液,所得溶液的pH及导电能力变化如图所示。下列叙述正确的是( )
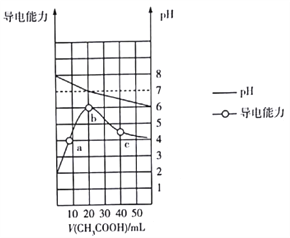
A. MOH是强电解质 B. b点对应的盐不水解
C. 水的离子积Kw:b>c>a D. c点溶液中c(CH3COO-)>c(M+)>c(H+)>c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com