
1)稀强酸、稀强碱反应生成1mol水时放出57.3 kJ的热。
① 实验室中可用稀盐酸和氢氧化钡稀溶液反应来测定中和热。请写出能表示该反应中和热的热化学方程式 ;
② 分别取100 mL 0.50 mol/L盐酸与100 mL 0.55 mol/L NaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。假设盐酸和氢氧化钠溶液的密度都是1g/cm3,中和后生成溶液的比热容c = 4.18 J/(g·℃)。实验时,测得反应前盐酸与NaOH溶液的平均温度为21.5℃,反应后混合溶液的温度为24.9℃。
则实验测得的中和热△H=____ ___(保留1位小数)
③ 如果用含1 mol CH3COOH的稀醋酸与足量稀氢氧化钠溶液反应,反应放出的热____57.3 kJ(填“大于”、“小于”或“等于”);理由是____________
(2)在催化剂的作用下CH4还原NO可以得到三种产物(该条件下均为气体),利用此反应能消除环境污染物NO。理论上每消耗标况下22.4 L NO就能放出290 kJ的热。写出该反应的热化学方程式
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
50℃和1.01×105 Pa时,该反应能自发进行:2N2O5(g) = 4NO2(g) + O2(g) △H= +56.76 kJ/mol,其自发进行的原因是( )
A.是吸热反应
B.是放热反应
C.是熵减少的反应
D.熵增大效应大于能量效应
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,将SO2和O2充入一密闭容器中,发生如下反应:2SO2(g)+O2(g) 2SO3(g)(正反应放热)反应过程中SO2、O2、SO3物质的量变化如图所示。回答下列问题:
2SO3(g)(正反应放热)反应过程中SO2、O2、SO3物质的量变化如图所示。回答下列问题:
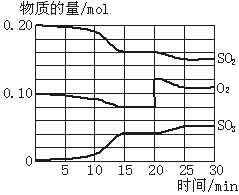 |
(1)降低温度,SO2的转化率_________,化学反应速率_________。(填“增大”“减小”或“不变”)
(2)反应处于平衡状态的时间是_____ ____。
(3)反应进行至20 min时,曲线发生变化的原因是_____________________ _(用文字表达)。
10 min到15 min的曲线变化的原因可能是_________(填写编号)。
a.加了催化剂 b.缩小容器体积
c.降低温度 d.增加SO3的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
用pH试纸测定无色溶液的pH时,规范的操作是
A.将pH试纸放入溶液中观察其颜色变化,跟标准比色卡比较
B.将溶液倒在pH试纸上,跟标准比色卡比较
C.用干燥的洁净玻璃棒蘸取溶液,滴在pH试纸上,跟标准比色卡比较
D.在试管内放入少量溶液,煮沸,把pH试纸放在管口,观察颜色,跟标准比色卡比
查看答案和解析>>
科目:高中化学 来源: 题型:
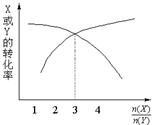
一定条件下,将X和Y两种气体按不同比例放入固定容积的密闭容器中,反应达平衡后,测得X、Y的转化率与起始时物质的量之比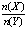 的关系如图。改变温度和压强,生成物Z的百分含量如表,则该反应的化学方程式可表示为
的关系如图。改变温度和压强,生成物Z的百分含量如表,则该反应的化学方程式可表示为
| 温度/℃ | 压强/kPa | Z的质量分数 |
| 200 | 101 | 0.40 |
| 300 | 101 | 0.48 |
| 400 | 202 | 0.52 |
| 400 | 303 | 0.52 |
A.3X(g)+Y(g) 4Z(g);ΔH>0 B.X(g)+3Y(g)
4Z(g);ΔH>0 B.X(g)+3Y(g) 4Z(g);ΔH>0
4Z(g);ΔH>0
C.3X(g)+Y(g) 3Z(g);ΔH<0 D.X(g)+3Y(g)
3Z(g);ΔH<0 D.X(g)+3Y(g) 3Z(g);ΔH<0
3Z(g);ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
世界气候大会与2009年在丹麦首都哥本哈根召开,商讨2012年至2020年全球温室气体减排协议。下列物质属于温室气体的是( )
A.可吸入颗粒 B.氮气 C.氧气 D.二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是 ( )
A.氢氧化钠溶液和稀盐酸反应:H++OH-===H2O
B.大理石与盐酸反应制取二氧化碳:CO32-+ 2H+=== H2O + CO2↑
C.铁粉投入FeCl3溶液中:Fe + Fe3+===2Fe2+
D.用小苏打治疗胃酸过多:CO32-+ 2H+===CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
扑热息痛是一种解热镇痛药,结构式为 。下列说法中错误的是
A.扑热息痛的分子式为C8H9NO2
B.扑热息痛可与烧碱溶液、浓溴水溶液发生反应
C.扑热息痛很稳定,不容易被氧化
D.扑热息痛核磁共振氢谱上有5个峰,峰面积之比为1︰1︰2︰2︰3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com