
分析 (1)加热条件下二氧化锰与浓盐酸反应生成氯化锰、氯气和水;
(2)根据n=$\frac{m}{M}$计算出二氧化锰的物质的量,再根据n=cV计算出100mL12mol/L浓盐酸中含有HCl的物质的量,结合反应方程式判断过量情况;
(3)根据不足量计算出生成氯气的物质的量,最后根据V=nVm计算出生成氯气在标准状况下的体积
(4)加入过量硝酸银溶液反应生成AgCl沉淀,根据Cl元素守恒可计算出生成氯化银的物质的量,然后根据m=nM计算出生成氯化银的质量.
解答 解:(1)加入二氧化锰与浓盐酸制取氯气,反应的化学方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,
答:发生反应为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)8.70gMnO2的物质的量为:$\frac{8.70g}{87g/mol}$=0.1mol,100mL12mol/L的浓盐酸中含有HCl的物质的量为:12mol/L×0.1L=1.2mol,
根据反应MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O可知,0.1mol二氧化锰完全反应消耗HCl的物质的量为:0.1mol×4=0.4mol<1.2mol,说明浓盐酸过量,
答:0.1mol二氧化锰完全反应消耗HCl的物质的量为:0.1mol×4=0.4mol<n(HCl)=1.2mol,说明浓盐酸过量;
(3)根据(2)可知生成的氯气按照二氧化锰的量计算,
MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O
1 1
0.1mol n(Cl2)
则生成氯气的物质的量为0.1mol,标准状况下0.1mol氯气的体积为:22.4L/mol×0.1mol=2.24L,
答:标准状况下生成Cl2的体积为2.24L;
(4)反应MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O中HCl被氧化生成氯气,根据Cl元素守恒可知发生氧化反应的HCl的物质的量为:n(HCl)=2n(Cl2)=0.1mol×
2=0.2mol,
100mL12mol/L的浓盐酸中含有HCl的物质的量为1.2mol,被氧化生成氯气的HCl的物质的量为0.2mol,则反应后溶液中含有氯离子的物质的量为:1.2mol-0.2mol=1.0mol,
根据Cl元素守恒可知生成AgCl的物质的量为1.0mol,质量为:143.5g/mol×1.0mol=143.5g,
答:向反应后的溶液中加入过量的AgNO3溶液,则能生成143.5gAgCl沉淀.
点评 本题考查化学方程式的计算,题目难度中等,正确判断过量情况为解答关键,注意掌握守恒思想在化学计算中的应用,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | ①②④⑥ | B. | ③④⑤⑥ | C. | ①③④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
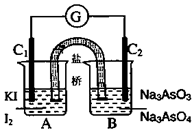 将AsO43-+2I-+2H+?AsO33-+I2+H2O设计成如图所示的电化学装置,其中C1、C2均为石墨棒.甲、乙两组同学分别进行下述操作:
将AsO43-+2I-+2H+?AsO33-+I2+H2O设计成如图所示的电化学装置,其中C1、C2均为石墨棒.甲、乙两组同学分别进行下述操作:| A. | 甲组操作过程中,C1做正极 | |
| B. | 乙组操作过程中,C2做负极,电极反应式为:AsO33-+2e-+2OH-=AsO43-+H2O | |
| C. | 两次操作过程中,微安表(G)指针的偏转方向相反 | |
| D. | 甲组操作时该装置为原电池,乙组操作时该装置为电解池 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 根据已学物质结构与性质的有关知识,回答下列问题:
根据已学物质结构与性质的有关知识,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | 某单质之一是空气中主要成分,最常见的助燃剂 |
| Y | 其某种核素不含中子 |
| Z | 失去一个电子后,形成Ne原子电子层结构 |
| W | 最外层电子数是次外层电子数的2倍 |
 、
、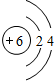 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔点、沸点:Li>Na>K>Rb>Cs | B. | 密度:Li<Na<K<Rb<Cs | ||
| C. | 原子半径:Li>Na>K>Rb>Cs | D. | 还原性:Li>Na>K>Rb>Cs |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧煤时加入适量石灰石,可减少废气中SO2的量 | |
| B. | 二氧化碳是“城市空气质量日报”报道内容之一 | |
| C. | pH在 5.6~7之间的降水通常称为酸雨 | |
| D. | 某雨水样品放置一段时间后pH减小是因为水中溶解的CO2增多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com