
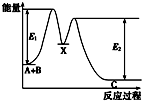
 反应A+B→C分两步进行:①A+B→X,②X→C,反应过程中能量变化如图所示,E4表示反应A+B→X的活化能,下列有关叙述正确的是( )
反应A+B→C分两步进行:①A+B→X,②X→C,反应过程中能量变化如图所示,E4表示反应A+B→X的活化能,下列有关叙述正确的是( )| A. | Ee表示反应X→C的活化能 | |
| B. | X是反应A+B→C的催化剂 | |
| C. | 反应A+B→C的△H<0 | |
| D. | 加入催化剂可改变反应A+B→C的焓变 |
分析 A.依据分子从常态转变为容易发生化学反应的活跃状态所需要的能量称为活化能;
B.依据催化剂是先作为反应物参与化学反应,然后再通过化学反应转变成原物质;
C.依据图象分析可知反应物AB能量高于生成物C的能量,反应是放热反应;
D.催化剂改变反应速率不改变化学平衡.
解答 解:A.反应②的活化能E1-E2,故A错误;
B.若X是反应A(g)+B(g)→C(g)的催化剂,则X是反应①的反应物,是反应②的生成物,故B错误;
C.图象分析可知反应物AB能量高于生成物C的能量,反应是放热反应,△H<0,故C正确;
D.焓变和反应物和生成物能量有关,与反应变化过程无关,催化剂只改变反应速率,不改变反应的焓变,故D错误;
故选C.
点评 本题考查了反应的焓变意义图象分析应用,催化剂改变反应速率的过程,掌握基础是关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
 如图所示,是原电池的装置图.请回答:
如图所示,是原电池的装置图.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
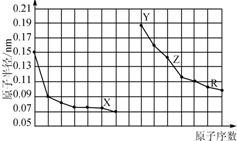
| A. | X、R的最高化合价相同 | |
| B. | 简单离子的半径:X>Y>Z | |
| C. | Y、Z、R对应的最高价氧化物的水化物相互之间可以发生反应 | |
| D. | 电解熔融的X与Z构成的化合物可以得到单质Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
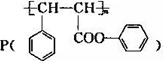 是一种环保型的新涂料,其合成路线如下图所示:
是一种环保型的新涂料,其合成路线如下图所示: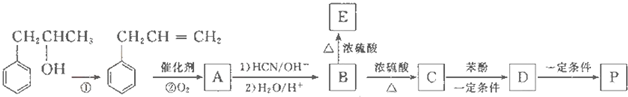
 .
. .
. .
. (写出其中一种的结构简式).
(写出其中一种的结构简式).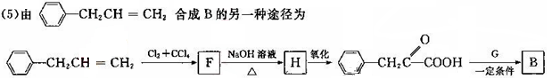
 ,试剂G的化学式H2.
,试剂G的化学式H2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.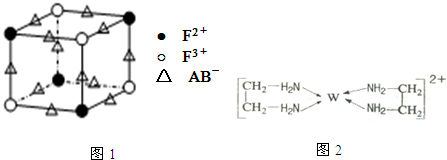
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 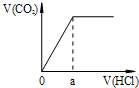 | B. | 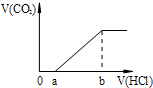 | ||
| C. | 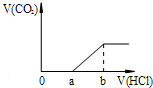 | D. | 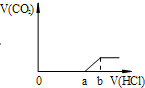 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾溶液具有强氧化性,可用作净水剂 | |
| B. | 二氧化硅不与任何酸反应,可用石英制造耐酸容器 | |
| C. | 铜的金属活动性比铁弱,可在海轮外壳上装若干铜块以减缓其腐蚀 | |
| D. | 常温下,铝能被浓硝酸钝化,可用铝制槽车运送浓硝酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com